1. ¿Qué es el SARS-CoV-2? responsable de Covid-19

Los coronavirus son virus de ARN no segmentados de la familia Coronaviridae y al orden Nidovirales distribuidos en humanos y otros mamíferos[1]. En la última década tres coronavirus altamente patógenos se han identificado, el causante del síndrome respiratorio de Medio Oriente (MERS-CoV en 2012), el coronavirus del síndrome respiratorio agudo severo (SARS en 2002–2003), y recientemente el SARS-CoV-2 agente causal de COVID-19 (Coronavirus Disease-2019[2]), estos ß-coronavirus han causado tres brotes zoonóticos, es decir, causan infecciones humanas cruzando los límites entre especies animales[3]. Esto se ha asociado a la venta de animales exóticos que indiscriminadamente se encuentran en los mercados para consumo, lo que propicia el desarrollo de nuevas variantes virales con potencial de causar infecciones graves[4].
La reciente pandemia que afecta a millones de personas en el mundo, es causada por el betacoronavirus SARS-CoV-2, identificado por el Centro Chino de control y prevención de enfermedades (Chinese Center for Disease Control and Prevention (CDC), el agente causal de la enfermedad respiatoria COVID-19[5]. De acuerdo a un análisis filogénetico el SARS-CoV-2 comparte un 96% de las identidades de secuencia de nucleótidos relacionado con al SARS (SL), RaTG descubierto en una cueva en Yunnan, China (2013), sin embargo, aún no es claro cuál es el reservorio de este virus[6].
El primer brote de COVID-19 se originó en Wuhan, provincia de Hubei en China en diciembre del 2019[6], donde se reportaron algunos casos inexplicables de neumonía. Inicialmente, se cuantificaron 27 pacientes que confirmaron esta enfermedad mediante métodos de secuenciación de próxima generación o PCR en tiempo real (RT-PCR). Para el 2 de enero el número de casos aumentó a 41, de los cuales, el 73% fueron de hombres, menos de la mitad del total de pacientes tenían además enfermedades subyacentes como la diabetes, hipertensión y afecciones cardiovasculares. Estos pacientes presentaron síntomas iniciales como fiebre, mialgia (dolor muscular) o fatiga, menos común la producción de esputo, cefalea (dolor de cabeza), hemoptisis (expectoración de sangre proveniente de los pulmones o los bronquios), diarrea, disnea (dificultad para respirar)[4], también se han reportado en pacientes con esta enfermedad cambios radiográficos en los pulmones, por ejemplo, en las imágenes de tomografía computarizada de tórax de un paciente hospitalizado con fiebre muy alta se compararon el día primero y cuatro días después de haber sido ingresado a hospitalización, las imágenes se presentan en la siguiente figura, donde en (a y c representan las imágenes de los pulmones del paciente al ingreso), se observaron sombras irregulares de alta densidad en el segmento dorsal del lóbulo inferior derecho (recuadros verdes), y (b, d) muestra las imagen obtenida 4 días después de la admisión del paciente, donde se detectaron sombras de alta densidad en forma de vidrio esmerilado en el segmento dorsal del pulmón derecho, y sombras irregulares en forma de nube de alta densidad y sombras de consolidación en el pulmón izquierdo (recuadros rojos[7]).
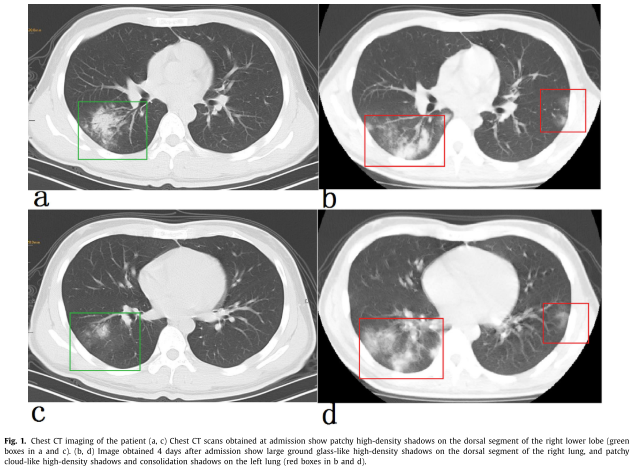
Otros síntomas de pacientes con COVID-19 son el recuento menor de linfocitos y plaquetas; hipoxemia (disminución anormal de la presión parcial de oxígeno en la sangre arterial, por debajo de 60 mmHg), y alteración de la función hepático-renal[8].
El COVID-19, es una enfermedad aguda que puede ser mortal, con una tasa de letalidad del 2%. Un daño alveolar masivo e insuficiencia respiratoria progresiva presentes en un estado avanzado de la enfermedad, son la causa de muerte en los pacientes infectados. Para el 15 de febrero, 66 580 casos y más de 1524 muertes se habían reportado en 26 países, aún sin patologías definidas debido a estudios postmorten limitados[9]. Datos reportados por la Organización Mundial de la Salud (OMS), al 27 de marzo confirman un total de casos de COVID-19 de 509164 y 23335 muertes por esta enfermedad; las cifras del número de casos progresivos adquiridos y de muertes por esta enfermedad en cada país se muestran en la URL https://apps.who.int/iris/bitstream/handle/10665/331613/nCoVsitrep27Mar2020-eng.pdf
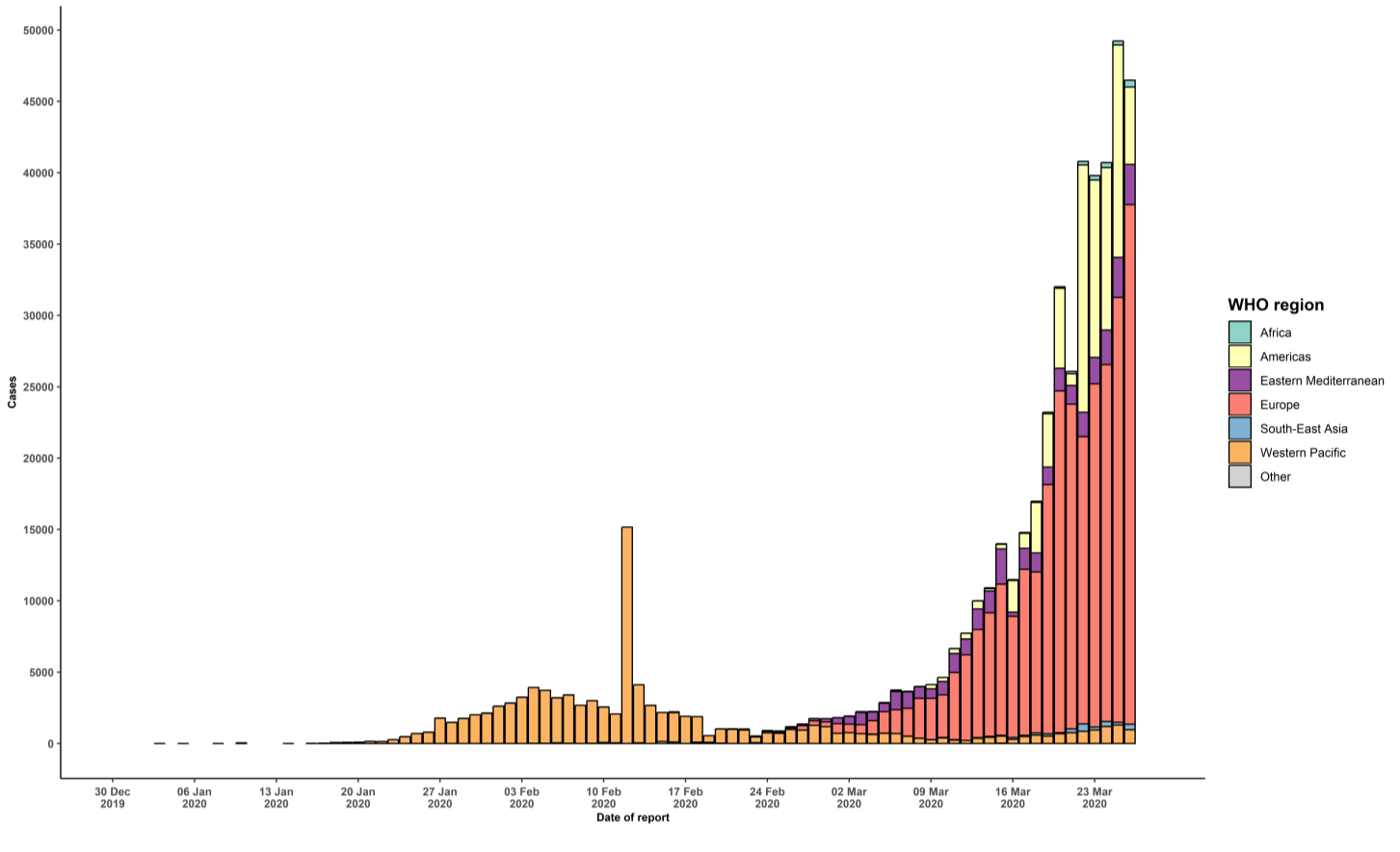
El 7 de enero, científicos chinos realizaron la secuenciación del genoma del 2019-nCoV; la secuencia genética se puso a disposición de la OMS el 12 de enero de 2020, esto facilitó realizar pruebas de diagnóstico de PCR para confirmar la enfermedad[10].

Diversas estrategias para el control y prevención de COVID-19 se están explorando en la comunidad científica, por ejemplo, el estudio de fármacos potenciales para combatir la enfermedad, aunque a la fecha no hay medicamentos antivirales con eficacia comprobada[11]; se utilizan las últimas tecnologías y métodos computacionales para edición del genoma, que incluye diagnóstico e identificación de blancos terapéuticos. Además, la obtención de una vacuna preventiva para esta enfermedad ocupa gran atención; se inició esta propuesta partiendo de la premisa de que el SARS-CoV-2 usa los mismos mecanismos de patogenicidad e invasión de las células del hospedero que su predecesor el SARS-CoV; ya que poseen secuencias genómicas casi idénticas y comparten una identidad de secuencia del 79,6%, la evidencia documental obtenida por Peng Zhou et al., (2020) se muestra en la siguiente figura[12]:
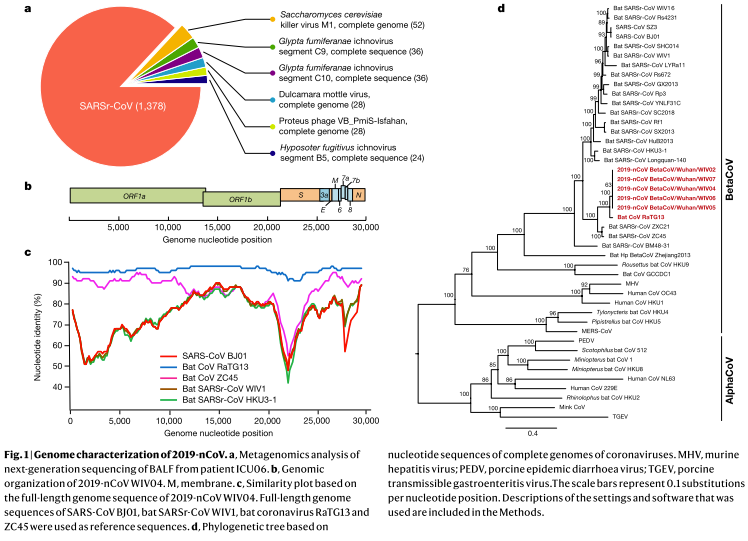
El mecanismo mediante el cual el SARS-CoV se une a su receptor para regular la fusión de la membrana, así como la entrada del virus a la célula es a través de glucoproteínas espiga (S1), las cuales se unen mediante su dominio C-terminal (dominio C) a su receptor[15], la enzima convertidora de angiotensina humana 2 (hACE2[13]), recientemente se demostró que tanto SARS-CoV como SARS-CoV-2 usan el mismo receptor de entrada celular, la hACE2[12].
A continuación mostramos un esquema de la estructura del SARS-CoV-2 y su invasión y posterior replicación de este virus en las células del hospedero, dicho esquema fue publicado en el Ney York Times por Jonathan Corum y Carl Zimme (Marzo 16, 2020) disponible en la URL: https://www.nytimes.com/es/interactive/2020/03/13/science/coronavirus-celulas-sintomas.html
1. Estructura típica de un coronavirus
El coronavirus recibe su nombre de las glicoproteínas de espiga que sobresalen de su superficie y se asemejan a una corona. El virus está envuelto en una burbuja grasosa de lípidos que se desintegra al contacto con el jabón.

2. Ingreso del coronavirus a una célula susceptible
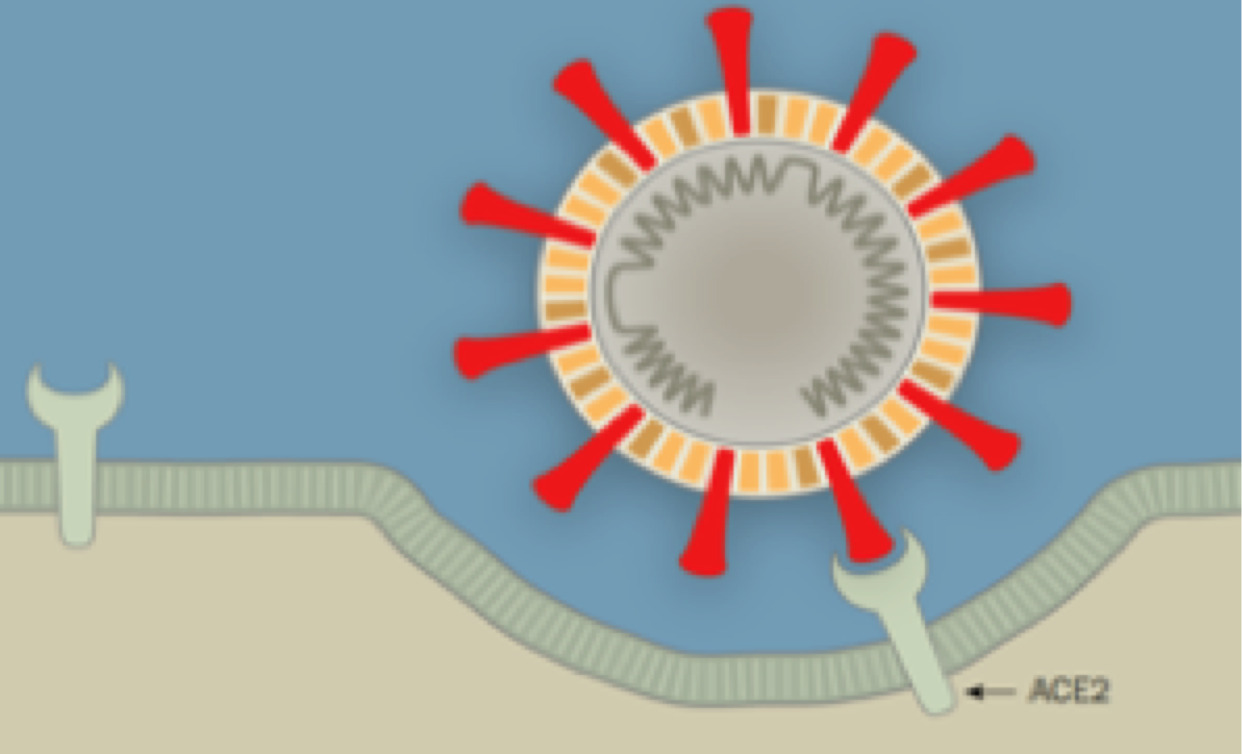
El virus entra al cuerpo a través de la nariz, la boca o los ojos y después se aferra a las células en las vías aéreas que producen una proteína llamada ACE2. Se cree que el virus se originó en los murciélagos, donde pudo haber estado adherido a una proteína similar.
3. Liberación de ARN viral
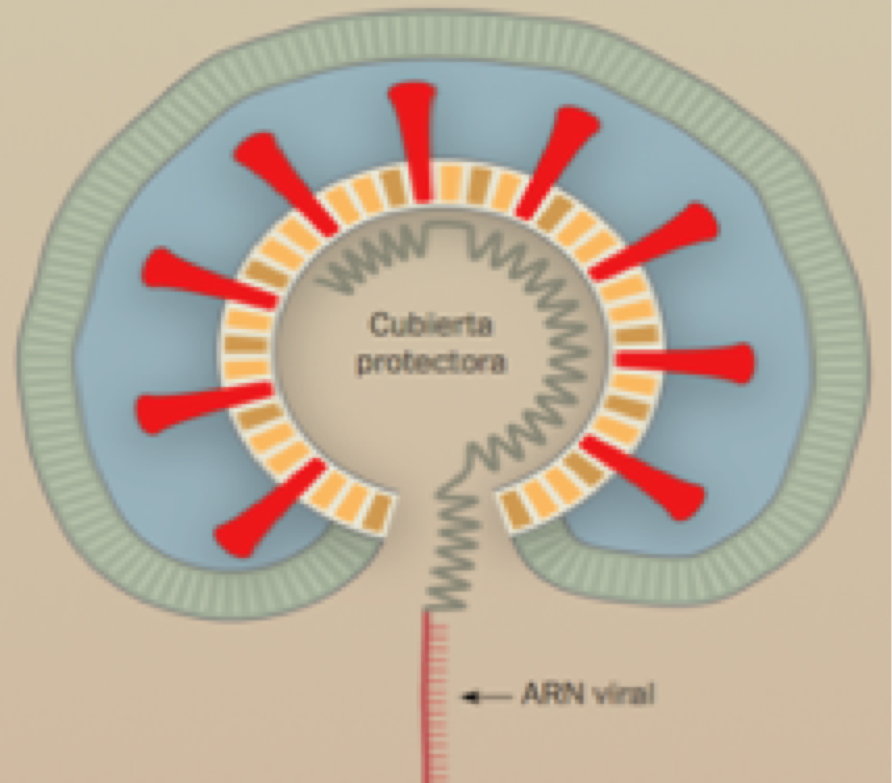
El virus infecta la célula al fusionar su membrana grasosa con la membrana de la célula. Una vez dentro el coronavirus libera un fragmento de material genético llamado ácido ribonucleico (ARN).
4. Secuestro de la célula
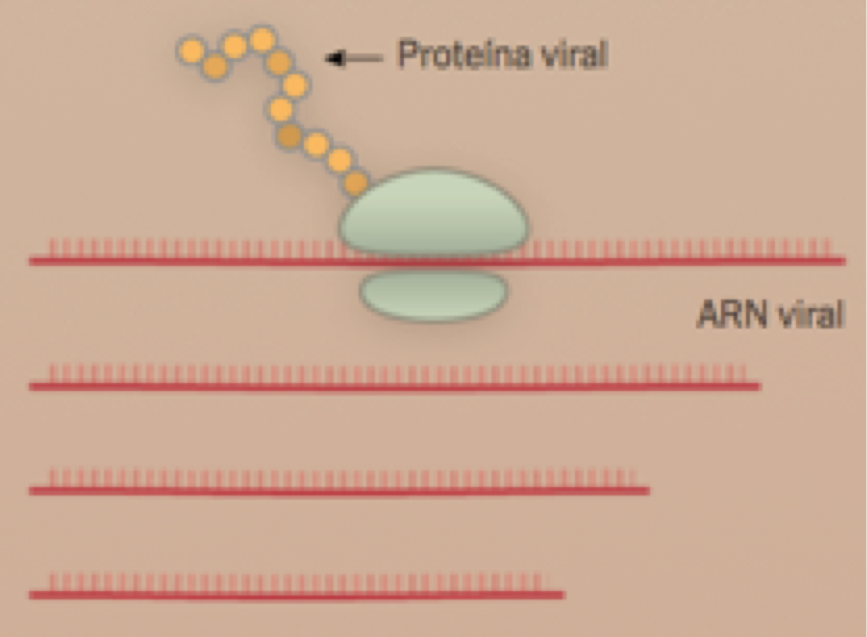
El genoma del virus tiene menos de 30.000 “letras” genéticas de longitud. (El nuestro, por ejemplo, tiene 3000 millones). La célula infectada lee el ARN y empieza a producir proteínas que mantienen al sistema inmunitario al margen y ayudan a crear nuevas copias del virus.
5. Fabricación de proteínas virales
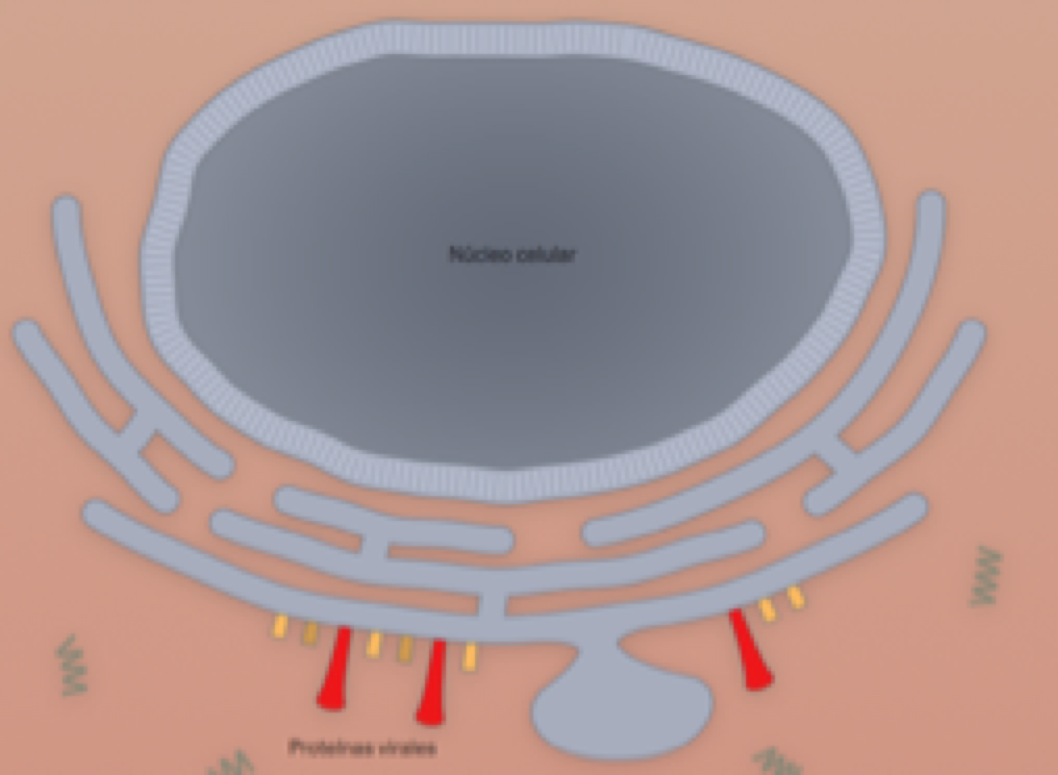
Conforme avanza la infección, la maquinaria de la célula empieza a producir nuevas espigas y otras proteínas que formarán más copias del coronavirus.
6. Ensamblado de nuevas copias
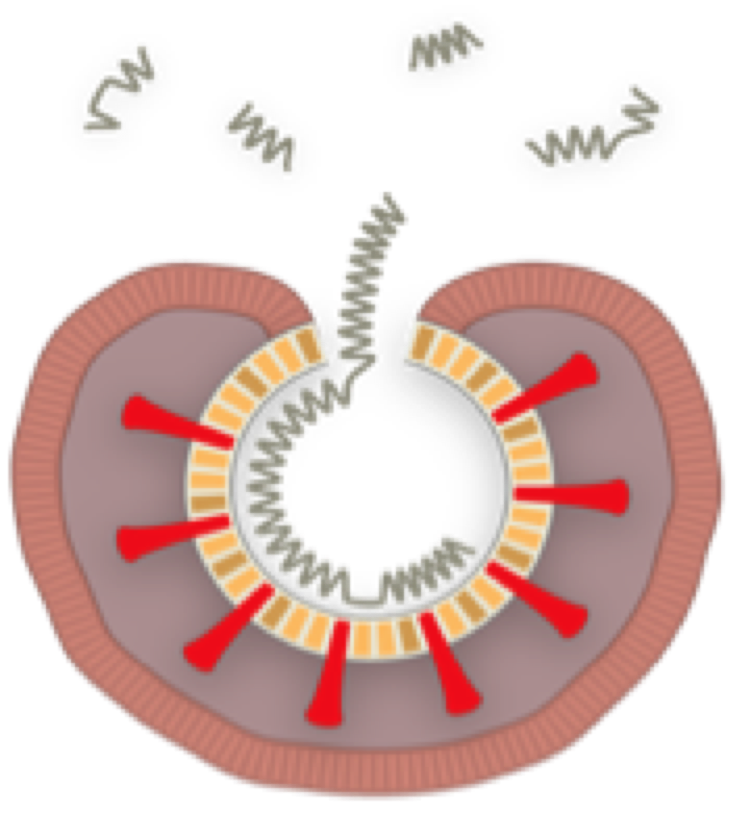
Las nuevas copias del virus se ensamblan y se transportan a los límites exteriores de la célula.
7. Propagación de la infección
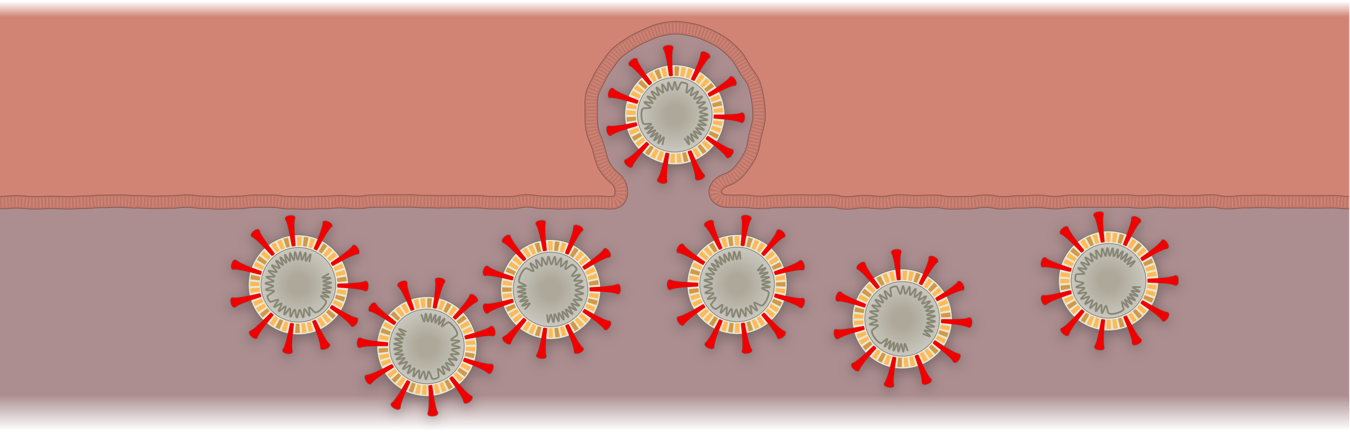
Cada célula infectada puede liberar millones de copias del virus antes de que la célula finalmente colapse y muera. Los virus pueden infectar las células vecinas o terminar en gotículas que escapan de los pulmones.
8. Respuesta inmunitaria
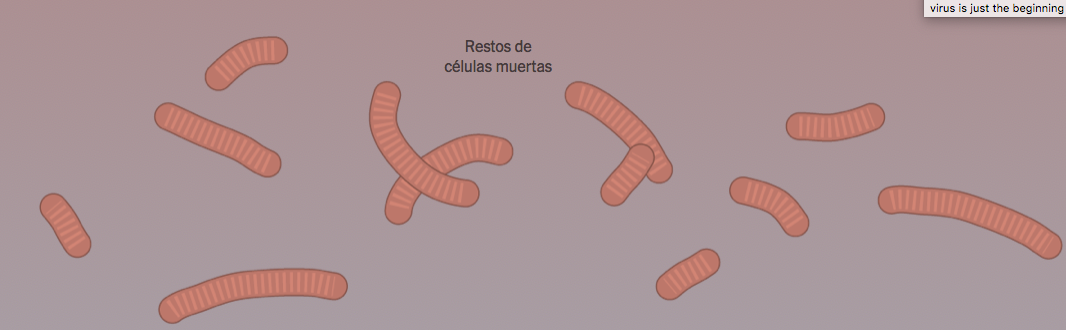
La mayoría de infecciones de COVID-19 causan fiebre porque el sistema inmunitario lucha para liberarse del virus. En casos severos, el sistema inmunitario puede sobrerreaccionar y empezar a atacar a las células pulmonares. Los pulmones se obstruyen con fluido y células moribundas, lo que dificulta la respiración. Un pequeño porcentaje de infecciones puede llevar al síndrome de dificultad respiratoria aguda y, posiblemente, la muerte.
9. Fuera del cuerpo
Al toser y estornudar se pueden expulsar gotículas llenas del virus en dirección de las personas y superficies cercanas, en donde el virus se mantiene infeccioso durante varias horas y hasta días. Los CDC recomiendan que las personas que han sido diagnosticadas con COVID-19 usen mascarillas para reducir la propagación de virus.
10. Una posible vacuna
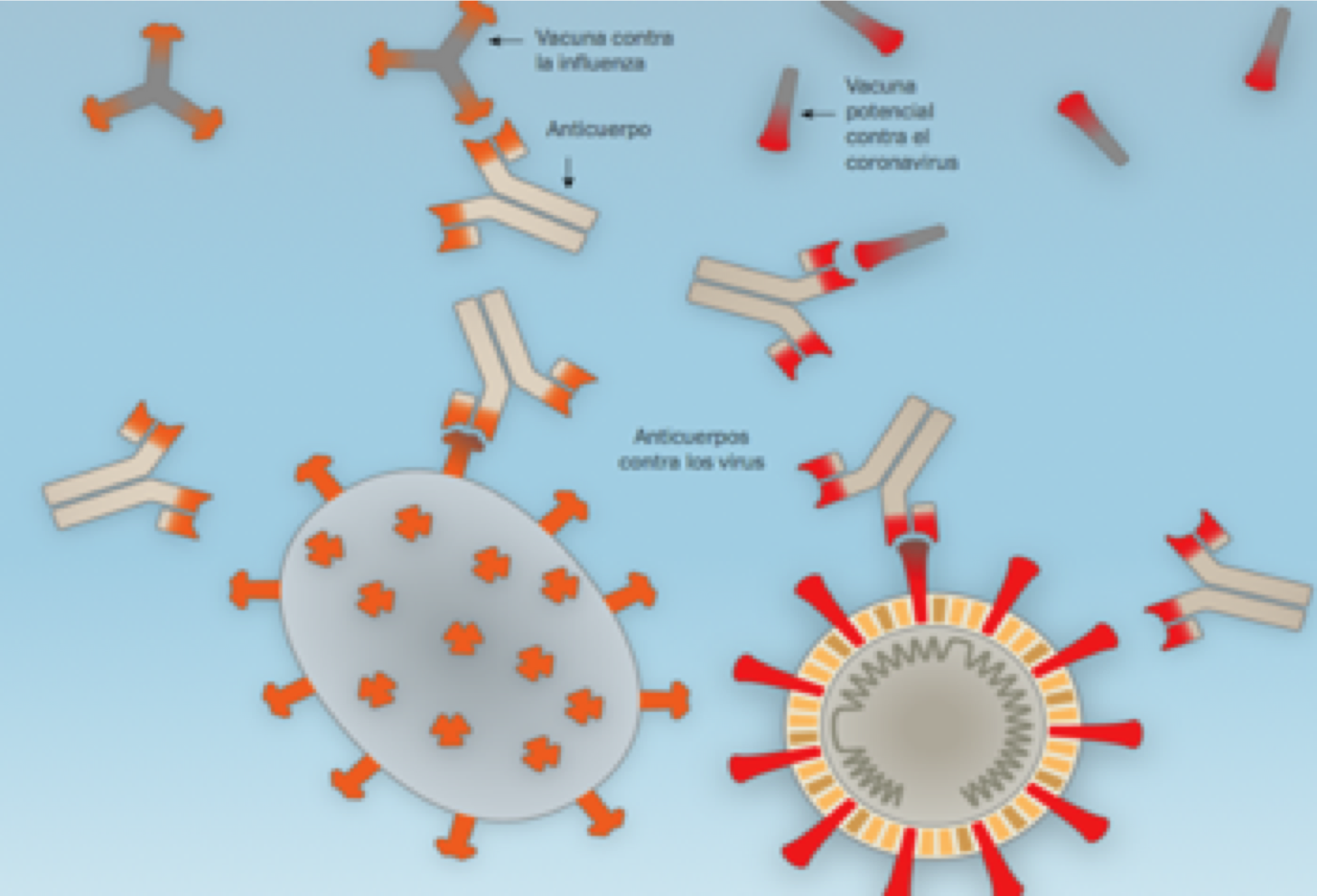
Una vacuna futura podría ayudar a que el cuerpo produzca anticuerpos contra el virus SARS-CoV-2 e impida que infecte las células humanas. La vacuna contra la influenza funciona de manera similar, pero los anticuerpos que se generan de la vacuna contra la influenza no protegen contra el coronavirus.
11. Cómo funciona el jabón
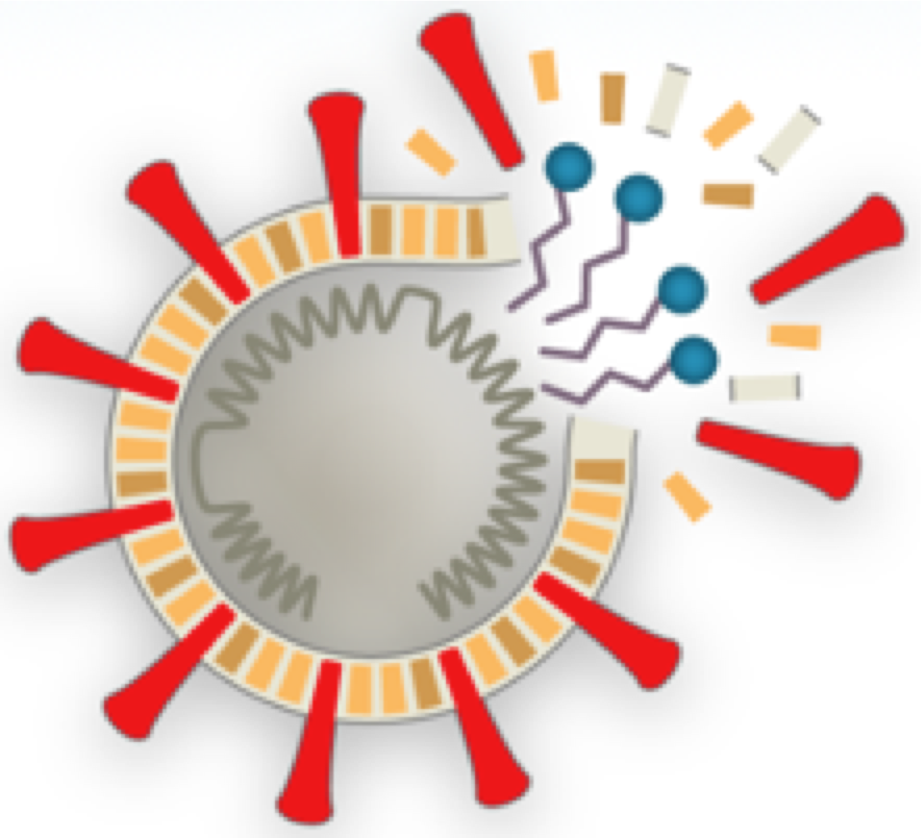
El jabón destruye el virus cuando las colas hidrófobas de las moléculas del jabón se adhieren a los lípidos de la membrana y la abren. La mejor forma de evitar infectarse con el coronavirus o con otros virus es lavarse las manos con jabón, evitar tocarse la cara, distanciarse de personas enfermas y limpiar con regularidad las superficies de mucho uso.
Referencias
[1] C. Huang, Y. Wang, X. Li, L. Ren, J. Zhao, Y. Hu, L. Zhang, G. Fan, J. Xu, X. Gu, Z. Cheng, T. Yu, J. Xia, Y. Wei, W. Wu, X. Xie, W. Yin, H. Li, M. Liu, Y. Xiao, H. Gao, L. Guo, J. Xie, G. Wang, R. Jiang, Z. Gao, Q. Jin, J. Wang, B. Cao, Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China, Lancet. 395 (2020) 497–506. doi:10.1016/S0140-6736(20)30183-5.
[2] W. Tai, L. He, X. Zhang, J. Pu, D. Voronin, S. Jiang, Y. Zhou, L. Du, Characterization of the receptor-binding domain (RBD) of 2019 novel coronavirus: implication for development of RBD protein as a viral attachment inhibitor and vaccine, Cell. Mol. Immunol. (2020). doi:10.1038/s41423-020-0400-4.
[3] X. Ou, Y. Liu, X. Lei, P. Li, D. Mi, L. Ren, L. Guo, R. Guo, T. Chen, J. Hu, Z. Xiang, Z. Mu, X. Chen, J. Chen, K. Hu, Q. Jin, J. Wang, Z. Qian, Characterization of spike glycoprotein of SARS-CoV-2 on virus entry and its immune cross-reactivity with SARS-CoV, Nat. Commun. 11 (2020). doi:10.1038/s41467-020-15562-9.
[4] G.A. Poland, Another coronavirus, another epidemic, another warning, Vaccine. 38 (2020) v–vi. doi:10.1016/j.vaccine.2020.02.039.
[5] David E. Gordon, Gwendolyn M. Jang, Mehdi Bouhaddou, Jiewei Xu, Kirsten Obernier, Matthew J. O’Meara, Jeffrey Z. Guo, Danielle L. Swaney, Tia A. Tummino, Ruth Huettenhain. A SARS-CoV-2-Human Protein-Protein Interaction Map Reveals Drug Targets and Potential Drug- Repurposing David, BioRxis. (2020). doi:doi.org/10.1101/2020.03.22.002386.
[6] H. Wang, Z. Wang, Y. Dong, R. Chang, C. Xu, X. Yu, S. Zhang, L. Tsamlag, M. Shang, J. Huang, Y. Wang, G. Xu, T. Shen, X. Zhang, Y. Cai, Phase-adjusted estimation of the number of Coronavirus Disease 2019 cases in Wuhan, China, Cell Discov. 6 (2020) 4–11. doi:10.1038/s41421-020-0148-0.
[7] W. Hao, Clinical Features of Atypical 2019 Novel Coronavirus Pneumonia with an initially Negative RT-PCR Assay., J. Infect. (2020) 4–5. doi:10.1016/j.jinf.2020.02.008.
[8] J.F.W. Chan, S. Yuan, K.H. Kok, K.K.W. To, H. Chu, J. Yang, F. Xing, J. Liu, C.C.Y. Yip, R.W.S. Poon, H.W. Tsoi, S.K.F. Lo, K.H. Chan, V.K.M. Poon, W.M. Chan, J.D. Ip, J.P. Cai, V.C.C. Cheng, H. Chen, C.K.M. Hui, K.Y. Yuen, A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster, Lancet. 395 (2020) 514–523. doi:10.1016/S0140-6736(20)30154-9.
[9] Z. Xu, L. Shi, Y. Wang, J. Zhang, L. Huang, C. Zhang, S. Liu, P. Zhao, H. Liu, L. Zhu, Y. Tai, C. Bai, T. Gao, J. Song, P. Xia, J. Dong, J. Zhao, F.S. Wang, Pathological findings of COVID-19 associated with acute respiratory distress syndrome, Lancet Respir. Med. 2600 (2020) 19–21. doi:10.1016/S2213-2600(20)30076-X.
[10] D.S. Hui, E. I Azhar, T.A. Madani, F. Ntoumi, R. Kock, O. Dar, G. Ippolito, T.D. Mchugh, Z.A. Memish, C. Drosten, A. Zumla, E. Petersen, The continuing 2019-nCoV epidemic threat of novel coronaviruses to global health — The latest 2019 novel coronavirus outbreak in Wuhan, China, Int. J. Infect. Dis. 91 (2020) 264–266. doi:10.1016/j.ijid.2020.01.009.
[11] S. Korea, We’re with you, Springer Nat. Ltd. 579 (2020) 471–2. The international journal of science / 26 March 2020 We’re.
[12] P. Zhou, X. Lou Yang, X.G. Wang, B. Hu, L. Zhang, W. Zhang, H.R. Si, Y. Zhu, B. Li, C.L. Huang, H.D. Chen, J. Chen, Y. Luo, H. Guo, R. Di Jiang, M.Q. Liu, Y. Chen, X.R. Shen, X. Wang, X.S. Zheng, K. Zhao, Q.J. Chen, F. Deng, L.L. Liu, B. Yan, F.X. Zhan, Y.Y. Wang, G.F. Xiao, Z.L. Shi, A pneumonia outbreak associated with a new coronavirus of probable bat origin, Nature. 579 (2020) 270–273. doi:10.1038/s41586-020-2012-7.
[13] W. Li, M.J. Moore, N. Vasilieva, J. Sui, Angiotensin-converting enzyme 2 is a functional receptor for the SARS coronavirus, Lett. to Nat. 426 (2003) 450–454. www.nature.com/nature.
_______________________________________________________________________________________
Autores:
Eduardo Ochoa Hernández
Gladys Juárez Cisneros
Nicolás Zamudio Hernández
Lizbeth Guadalupe Villalon Magallan
Rogelio Ochoa Barragán