Texto universitario

_____________________________
CAPÍTULO 8. Espectroscopía de infrarrojo y Raman
8.1 Introducción
La espectroscopía de infrarrojo (IR) se refiere a la medición de la absorción de diferentes frecuencias de radiación IR por alimentos u otros sólidos, líquidos o gases. La espectroscopía IR comenzó en 1800 con un experimento por Herschel. Cuando usó un prisma para crear un espectro a partir de luz blanca, y colocó un termómetro en un punto justo más allá de la región roja del espectro observando un aumento en la temperatura. Esta fue la primera observación de los efectos de la radiación IR[1].
En la década de 1940, la espectroscopía IR se había convertido en una herramienta importante utilizada por los químicos para identificar los grupos funcionales en compuestos orgánicos. En la década de 1970, se introdujeron instrumentos comerciales de reflectancia cerca del IR (NIR) que proporcionaron rápidamente determinaciones cuantitativas de humedad, proteínas y grasas en granos de cereales y otros alimentos. Hoy en día, la espectroscopía IR se utiliza ampliamente en la industria alimentaria para análisis cualitativos y cuantitativos de ingredientes y alimentos terminados. En este capítulo, se describen las técnicas de espectroscopía de IR y Raman media y cercana, incluidos los principios por los cuales las moléculas absorben la radiación IR, los componentes y la configuración de espectrómetros IR comerciales, métodos de muestreo para la espectroscopía IR y aplicaciones cualitativas y cuantitativas de estas técnicas para el análisis de alimentos.
8.2 Principios de espectroscopía IR
8.2.1 La región IR del espectro electromagnético
Es la energía electromagnética con longitudes de onda (λ) más largas que la luz visible, pero más cortas que las de microondas. Por lo general, las longitudes de onda de 0.8 a 100 micrómetros (µm) se pueden utilizar para la espectroscopía IR y se dividen en el IR cercano (0.8-2.5 µm; 12500-400 cm-1), las regiones de medio IR (2.5 a 15.4 µm; 4000-650 cm-1) y las regiones de infrarrojos lejanos (15.4-100 µm ;650-100 cm-1). Un µm es igual a 1 x 10-6 m. Las regiones de infrarrojo cercano y medio del espectro son más útiles para el análisis cuantitativo y cualitativo de los alimentos[2].
La radiación IR también se puede medir en términos de su frecuencia, lo que es útil porque la frecuencia está directamente relacionada con la energía de la radiación por la siguiente relación:
E= hv (8.1)
Donde
E= Energía del sistema h= Constante de Planck V= Frecuencia en Hertz
Las frecuencias se expresan comúnmente como números de onda (?, en centímetros recíprocos, cm-1). Donde los números de onda se calculan como se ilustra a continuación:
? = 1/(λ in cm) = 104/(λ in µm) (8.2)
8.2.2 Vibraciones moleculares
Una molécula puede absorber la radiación IR si vibra en tal manera que su distribución de la carga, y por lo tanto su momento dipolo eléctrico, cambia durante la vibración. Aunque hay muchas vibraciones posibles en una molécula poliatómica, las vibraciones más importantes que producen un cambio en el momento dipolo son estiramientos (simétrico y asimétrico) y flexiones (tijera, mecedor, torsión, menguante). Ejemplos de estas vibraciones para la molécula de agua se muestran en la Fig. 8.1. Tenga en cuenta que los movimientos de estiramiento las moléculas vibran a frecuencias más altas que el movimiento de tijera. Además, los estiramientos asimétricos son más propensos a un cambio en el momento del dipolo, con absorción de radiación IR, que las simétricas.
8.2.3 Factores que afectan a la frecuencia de la vibración
El requisito básico para la absorción de la radiación infrarroja es que debe haber un cambio neto en el momento dipolo durante la vibración de la molécula o grupo funcional. Se puede pensar en una vibración molecular como un oscilador armónico (Fig. 8.2a), con el nivel de energía para cualquier vibración molecular dada por la siguiente ecuación:
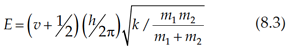
Donde:
v= Número cuántico vibratorio (número entero positivo valores, incluyendo cero, solamente)
h= La constante de Planck
k= Fuerza constante del enlace
m1 y m2: masas de los átomos individuales involucrados en la vibración
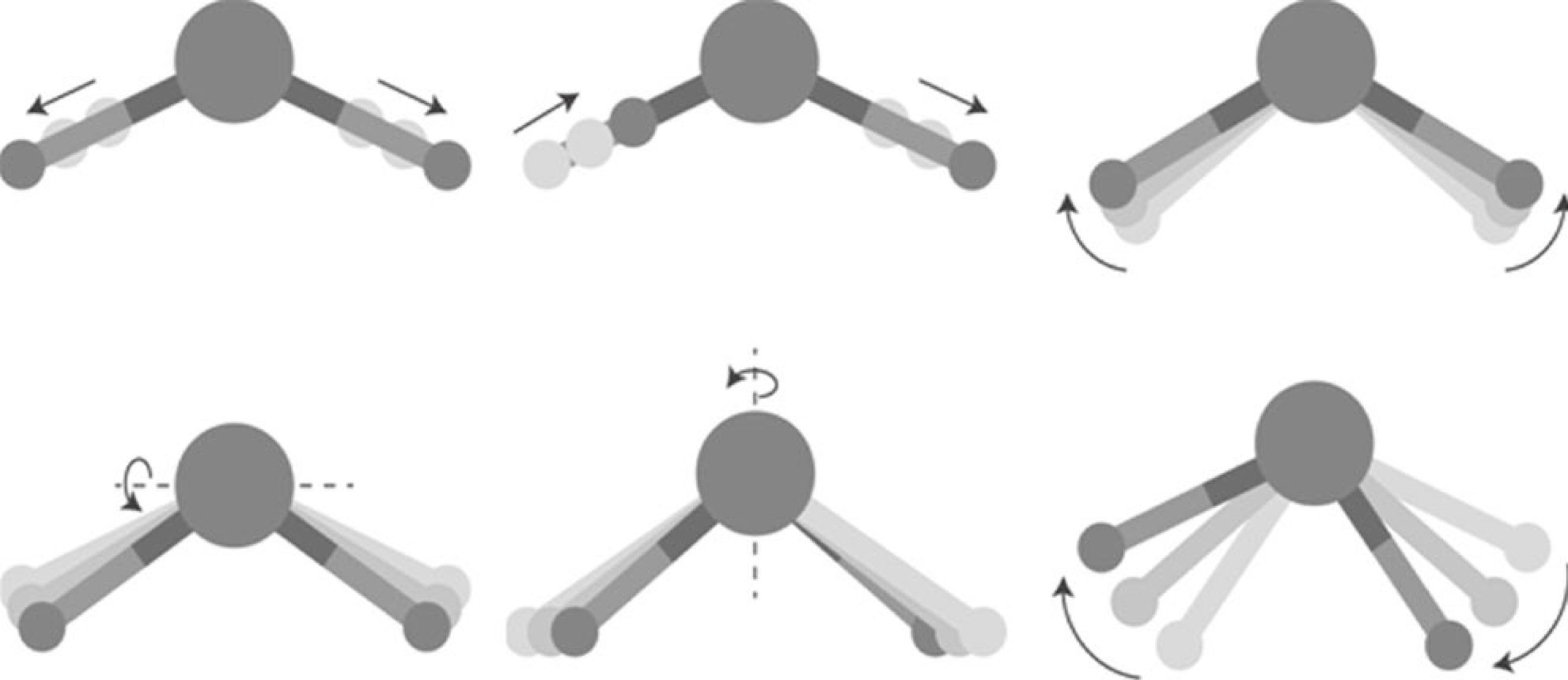
Figura 8.1 Modos vibracionales de una molécula de agua.
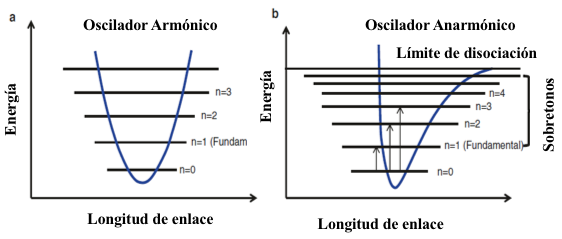
Figura 8.2 Diagrama de las diferencias en las curvas de energía potencial entre el modelo de oscilador (a) armónico y (b) anarmónico.
Tenga en cuenta que la energía vibratoria, y por lo tanto la frecuencia de vibración, es directamente proporcional a la fuerza del enlace e inversamente proporcional a la masa del sistema molecular. Por lo tanto, los grupos funcionales vibrarán a diferentes frecuencias. Un grupo molecular funcional vibratorio puede absorber energía radiante para moverse de la vibración más baja (v= 0) a un estado excitado (v =1), y la frecuencia de radiación que hará que esto ocurra es idéntica a la frecuencia inicial de vibración del enlace. Esta frecuencia es referida como la Absorción fundamental. El oscilador armónico proporciona una buena explicación uniendo las vibraciones de estiramiento para vibraciones fundamentales. Sin embargo, las moléculas también pueden absorber radiación para pasar a un estado excitado más alto (v= 2 o 3), de tal forma que la frecuencia de la radiación absorbida sea dos o tres veces mayor que la frecuencia fundamental. Estas absorciones se conocen como armónicos, y las intensidades de estas absorciones son mucho más bajas que las fundamentales ya que estas transiciones son menos favorecidas. El modelo de oscilador anarmónico (Fig. 8.2b) representa la repulsión y atracción de la nube del electrones nube acomodando la disociación de enlaces en niveles de energía. En general, las vibraciones fundamentales no se ven afectadas por los términos de anarmonía, pero con matices las transiciones están influenciadas por la anarmonía, pero las transiciones están influenciadas por la anarmonocidad, que debe tenerse en cuenta a la hora de evaluar la frecuencia de estas vibraciones de mayor frecuencia. Las combinación de bandas también puede ocurrir si dos o más vibraciones interactúan para dar bandas que son sumas de sus frecuencias fundamentales. El modelo de la oscilación armónico y su modificación para tener en cuenta la anarmonicidad permite explicar el origen de muchas de las frecuencias características que pueden ser combinaciones particulares de átomos dentro de un molécula. El resultado general es que cada grupo funcional en el centro de la molécula absorbe la radiación IR en distintas bandas de longitud de onda en lugar de mostrar una continuidad.
8.3 Espectroscopía Mid-IR
La espectroscopía de infrarrojos medio mide la capacidad de una muestra para absorber la luz en la región de 2,5–15 µm (4000–650 cm-1). Las absorciones fundamentales se observan principalmente en esta región espectral. La espectroscopía de infrarrojo medio es muy útil en el estudio de compuestos orgánicos porque las bandas de absorción están relacionadas con los modos vibratorios de grupos funcionales específicos. El posicionamiento de la banda y su intensidad están correlacionadas con la energía del enlace, su entorno y su concentración en la matriz, por lo que la espectroscopía de infrarrojo medio es ideal para ambas aplicaciones cualitativas y cuantitativas[3].
8.3.1 Instrumentación
8.3.1.1 Visión general
Hay dos tipos de espectrómetros disponibles para el análisis de IR medio, dispersivo y de transformación de Fourier (FT). Los sistemas dispersivos han estado disponibles desde la década de 1940 utilizando prismas o rejillas como elementos dispersivos. Estos sistemas contienen componentes similares a los espectrómetros ultravioleta-visibles (UV-Vis), incluyendo una fuente de radiación, un monocromador, un portamuestras, y un detector conectado a un amplificador del sistema para grabar los espectros. En estos sistemas, un filtro, rejilla o prisma se utiliza para separar la radiación IR en sus longitudes de onda individuales. Un avance en el campo de la espectroscopía de IR medio fue el desarrollo de espectrómetros infrarrojos de transformación de Fourier (FTIR), que han sustituido primordialmente a los instrumentos debido a la mejora drástica en la calidad de los espectros y la disminución del tiempo necesario para obtener datos.
8.3.1.2 Instrumentos de transformación de Fourier
En comparación con los instrumentos dispersivos de infrarrojo medio, los espectrómetros FTIR en el análisis de alimentos permiten una mayor velocidad, sensibilidad, y resolución superior de la longitud de onda, y la precisión de la longitud de onda. En los instrumentos de transformación de Fourier (FT), la radiación no se dispersa, sino que las longitudes de onda llegan al detector simultáneamente, se utiliza un procesamiento matemático para convertir la resultados en un espectro IR típico.
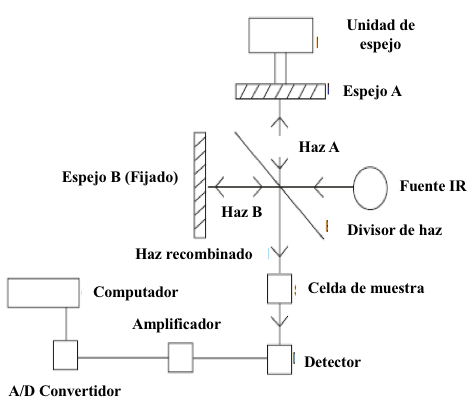
Figura 8.3 Diagrama de bloques de un interferómetro y los electrónicos asociados típicamente usados en un instrumento FTIR.
En lugar de un monocromador, el instrumento utiliza un interferómetro. El interferómetro Michelson es el más utilizado, y su mecanismo es simple (Fig. 8.3). La radiación infrarroja de la fuente se divide en dos por un divisor de haz, y cada mitad de la viga va a un espejo (ya sea un espejo fijo o en movimiento). En los haces se reflejan hacia atrás y se recombinan en la viga que resulta en interferencias dirigidas a la muestra (o referencia) y luego al detector. El movimiento del espejo móvil da como resultado el cambio de trayectoria óptico de longitud entre las dos vigas divididas de modo que se crean interferencias constructivas, destructivas e intermedias (siendo dominante la interferencia destructiva). La salida resultante se conoce como interferograma, que es la intensidad medida por el detector como función de la posición del espejo en movimiento. Cuando una muestra interactúa con el haz recombinado por delante del detector, las moléculas absorben IR en sus frecuencias características, y por lo tanto la radiación que llega al detector se modifica (Fig. 8.4). Una vez que se recopilan los datos, un transformación matemática llamada "transformación de Fourier" convierte el interferograma del dominio del tiempo (intensidad versus tiempo) en un espectro IR en la frecuencia dominio (intensidad frente a frecuencia). Una computadora permite que la transformación matemática sea completada rápidamente[4].
Las fuentes de radiación comunes para los espectrómetros de infrarrojo medio son sólidos inertes calentados eléctricamente a 1000–1800 °C. Tres tipos populares de fuentes son los Nernst (construidos con óxidos de tierras raras), Globar (construidos de carburo de silicio), y una bobina de nicromo envuelto alrededor de un núcleo de cerámica que brilla cuando una corriente eléctrica pasa a través de ella. Todos producen radiación continua, pero una radiación con diferentes perfiles de energía.
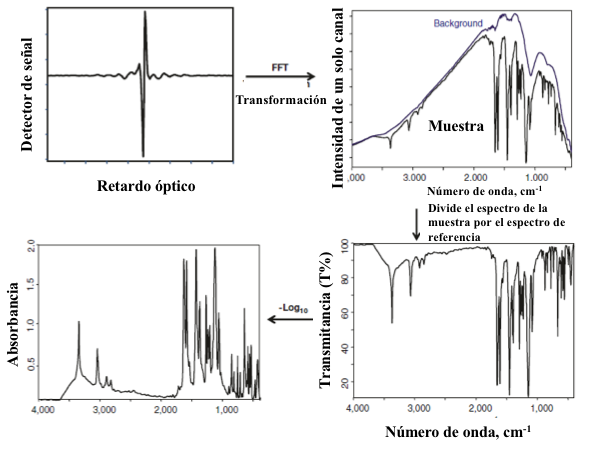
Figura 8.4 Ilustración del proceso de convertir un inferograma a un espectro de infrarrojo usando el algoritmo de transformación de Fourier.
Los detectores incluyen termopares para los cuales el voltaje de salida varía con los cambios de temperatura causados por niveles variables de radiación que incide en el detector. En un detector Golay, la radiación incide en un tubo sellado de gas xenón que calienta el gas y provoca un aumento de presión dentro del tubo. Sin embargo, la mayoría de los instrumentos modernos usan detectores piroeléctricos, como el de cristales de sulfato de triglicina deuterado (DTGS) o detectores semiconductores de estado sólido. La variación en la cantidad de radiación que incide en un detector DTGS provocan un cambio en la temperatura del detector, lo que resulta un cambio dieléctrico constante del elemento DTGS. El resultado se mide en el cambio de la capacidad semiconductora de los detectores, como los hechos de mercurio – cadmio– aleación de telurio (MCT), tienen conductividades que varían según la cantidad de radiación que incide en la superficie del detector. Los detectores MCT responden a cambios más rápidos en la intensidad de radiación que otros detectores; sin embargo, generalmente requieren enfriamiento criogénico. Los detectores DTGS y MCT son los detectores más utilizados en los instrumentos que emplean la transformada de Fourier
8.3.2 Técnicas de manipulación de muestras
El modo de transmisión se basa en el paso del haz IR a través de una muestra que se coloca entre dos ventanas transparentes de IR. Los líquidos a menudo se miden por espectroscopía IR de transmisión. Porque los coeficientes de absorción en el IR medio son altos, las celdas que poseen longitudes de trayectoria de solo 0.01–1.0 mm son comúnmente usadas. El cuarzo y el vidrio absorben en la región del IR medio, así que las ventanas de las celdas están hechas de materiales tales como sales de haluro o sulfuro. Las sales de haluro son solubles en agua, y se debe tener cuidado al seleccionar celdas para usarse con muestras acuosas. También están disponibles con ventanas hechas de materiales duraderos y menos solubles, como seleniuro de zinc, pero son más caros que los que contienen ventanas de sales de haluro. Las celdas líquidas deben estar libres de burbujas de aire y se debe tener especial cuidado al limpiar entre el uso de distintas muestras.
Los espectros de transmisión de sólidos se pueden obtener moliendo finamente una pequeña cantidad de la muestra con bromuro de potasio (KBr), presionando la mezcla en un pellet bajo alta presión e insertando el pellet en el rayo IR. Las limitaciones de esta técnica incluyen dificultad para manipular y almacenar un KBr higroscópico y la complejidad y tiempo necesarios para hacer un buen pellet KBr. Una técnica alternativa es dispersar un sólido finamente dividido en aceite mineral Nujol para formar un momento de reflexión.
Los espectros de transmisión de muestras gaseosas se pueden obtener usando una celda de vidrio sellada de 2–10 cm y ventanas transparentes IR. Para el análisis de trazas de paso múltiple hay celdas disponibles que reflejan el haz IR hacía atrás y hacia adelante a través de la celda muchas veces para obtener la trayectoria de las longitudes de hasta varios metros. Los instrumentos FTIR también se pueden conectar a un cromatógrafo de gases, para obtener espectros de compuestos que eluyen de la columna de cromatografía.
La reflectancia total atenuada (ATR) es una técnica de muestreo ampliamente aplicada en espectroscopía de infrarrojo, porque requiere poca o ninguna preparación de la muestra, elimina la variación en la longitud de la trayectoria a la celda y proporciona una colección de espectros consistente. La ATR permite obtener espectros de muestras sólidas que son demasiado gruesas para las mediciones por transmisión, por ejemplo, pastas como la mantequilla de maní y líquidos viscosos. La ATR funciona basado en el efecto de atenuación de la luz infrarroja (Fig. 8.5) cuando está dirigido a una interfaz entre una reflexión interna de un elemento (cristal) con propiedades de alto índice de refracción (es decir, seleniuro de zinc (ZnSe), yoduro de talio-talio bromuro (KRS-5), germanio (Ge), silicio (Si) y diamante) y un material de bajo índice de refracción (muestra de alimentos) en su superficie. Sobre la interacción con la superficie reflectante, la radiación llamada onda evanescente se forma en el material de alto índice de refracción, y penetra ligeramente en la muestra. La muestra absorbe selectivamente, la intensidad de la radiación reflejada, es reducida a las longitudes de onda características para que la muestra absorba radiación, y la radiación atenuada final que sale del cristal se mide como única para la muestra analizada.
La radiación no se transmite a través de la muestra; por lo tanto, no hay necesidad de que la muestra sea delgada para permitir la transmisión de la luz incidente. Dado que la profundidad de penetración de la radiación es limitada a unos pocos micrómetros (μm), el mismo espectro es obtenido independientemente de la cantidad de la muestra colocado en la superficie, y no hay necesidad de diluir la muestra.
El estado físico de la muestra es un importante factor, porque debe estar en contacto íntimo con el Cristal ATR para obtener un buen espectro ATR. Los líquidos y las pastas generalmente exhiben mejores espectros ATR que las muestras sólidas Se utiliza un sistema de sujeción por presión.
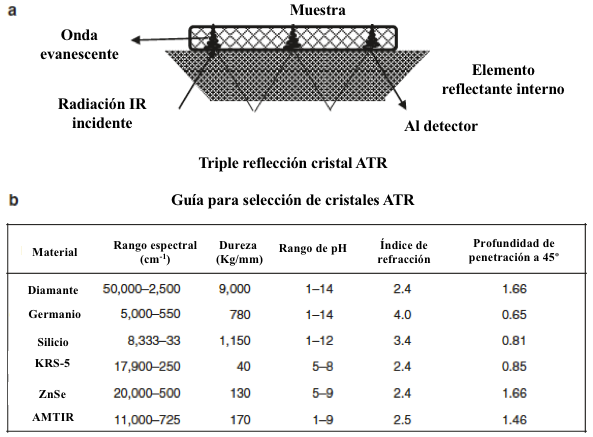
Figura 8.5 (a) Ilustración del fenómeno de reflexión en una reflexión accesoria de una reflexión total triple atenuada y la formación de una onda evanescente dentro de la muestra. (b) Características de cristales ATR.
8.3.3 Aplicaciones de la espectroscopía de IR medio
8.3.3.1 Bandas de absorción de grupos funcionales orgánicos
La espectroscopía de infrarrojo monitorea la interacción de los grupos funcionales en moléculas químicas con luz infrarroja que resulta en vibraciones predecibles que proporcionan una "Huella digital" característica de sustancias químicas presentes en la muestra. Los espectros en la región del medio IR tienen bandas bien definidas que se pueden ser asignadas a grupos funcionales presentes en los componentes de los alimentos[5]. El posicionamiento de la banda facilita la caracterización estructural, y su intensidad se correlaciona con su concentración en la matriz, permitiendo tanto cualitativa como cuantitativamente sus aplicaciones.
Los espectros se presentan comúnmente en números de onda graficados en el eje x y el porcentaje de transmitancia o absorbancia trazada en el eje y. Los espectros de IR medio de alimentos seleccionados se muestran en la figura 8.6 mostrando las principales bandas de absorción que pueden asociarse con grupos funcionales (Tabla 8.1) en grasas, proteínas y productos ricos en carbohidratos.
El perfil espectral único se puede utilizar para identificar grupos funcionales específicos presentes en una sustancia desconocida. Comparando el espectro IR medio con un conjunto de espectros estándar y determinar la coincidencia más cercana se puede lograr la identificación de compuestos químicos.
Las bibliotecas espectrales están disponibles en varias fuentes, pero probablemente la mayor colección de normas es la Sadtler Standard Spectra (División Sadtler de Bio-Rad Inc., Philadelphia, PA) que contiene más de 225,000 espectros de infrarrojo. Los algoritmos se utilizan para comparar el espectro desconocido para cada espectro en la base de referencia de datos y se determina el impacto del índice de calidad (HQI), indicando la similitud entre espectros. Se pueden generar varios valores HQI para los compuestos desconocidos, y el software clasificará y mostrará las mejores coincidencias en un informe de búsqueda. El ruido y artefactos pueden afectar el HQI y provocar errores en la identificación; Por lo tanto, es imprescindible realizar comparaciones visuales para confirmar un buen partido espectral. Las búsquedas se realizarán con mayor frecuencia en sustancias purificadas, en lugar de alimentos o productos básicos.
8.3.3.2 Aplicaciones
Las mediciones espectroscópicas de IR medio obedecen la ley de Beer, aunque las desviaciones pueden ser mayores que en la espectroscopía UV-Vis debido a las bajas intensidades de las fuentes de IR, las bajas sensibilidades de los detectores de IR y la relativa estrechez de las bandas de absorción de IR medio. El primer y más extenso uso de esta técnica es el analizador de leche por infrarrojo, que tiene la capacidad de analizar cientos de muestras por hora. La grasa, la proteína, y el contenido de lactosa de la leche se pueden determinar simultáneamente con uno de estos instrumentos. El éster carbonilo y los grupos de lípidos absorben a 5,73 μm (1742 cm− 1), los grupos amida de proteína absorben a 6.47 μm (1545 cm− 1), y los grupos hidroxilo de lactosa absorben a 9.61 μm (1045 cm− 1). Estos instrumentos automatizados homogenizan los glóbulos de grasa de la leche para minimizar la dispersión de luz por el muestreo y luego bombean la leche en una celda de flujo a través de la cual se pasa el haz IR. El instrumento se calibra utilizando muestras de concentración conocidas para establecer la pendiente y la intercepción.
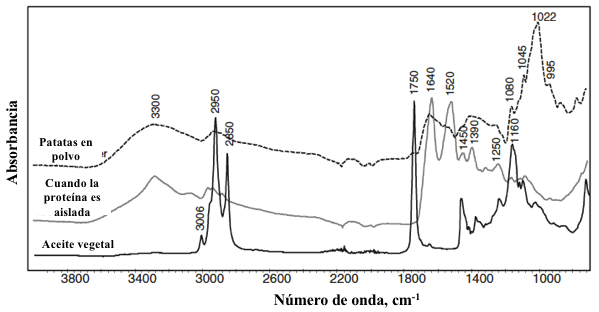
Figura 8.6 Espectro de IR medio de aceite de maíz, proteína de suero aislada, y harina de patatas medidos por una unidad de triple reflexión ATR. La frecuencia en números de onda e intensidad son expuestos en el eje x.
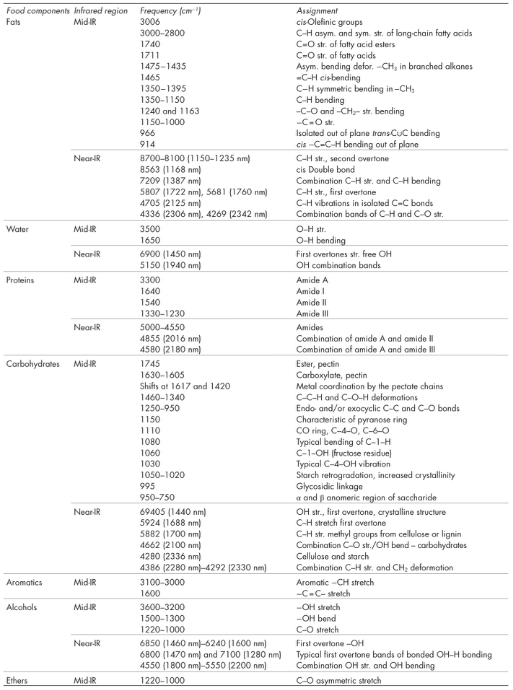
Tabla 8.1 Frecuencias características de absorción de IR medio y cercano de los principales componentes de los alimentos.
Se han adoptado métodos oficiales para los analizadores de leche IR y procedimientos específicos para el funcionamiento de estos instrumentos. Hay muchas aplicaciones adicionales de espectroscopía de IR medio para análisis de alimentos. Debido a la naturaleza compleja de los espectros infrarrojos, las técnicas de análisis estadístico multivariante (Quimiometría) a menudo se debe utilizar para extraer información de los espectros infrarrojos, lo que permite la clasificación y análisis cuantitativo de múltiples componentes en alimentos.
8.4 Espectroscopía de IR cercano
Mediciones en la región espectral de IR cercano (NIR) (0.7–2.5 μm, igual a 700–2500 nm) son más ampliamente utilizadas para el análisis cuantitativo de alimentos que las mediciones del IR medio. Varios instrumentos comerciales están disponibles para el análisis de composición de alimentos usando espectroscopía de infrarrojo cercano. Una gran ventaja del IR cercano es su capacidad de medir directamente la composición de productos alimenticios sólidos mediante el uso difuso de técnicas de reflexión.
8.4.1 Principios
8.4.1.1 Principios de mediciones de reflexión difusa
Cuando la radiación golpea un material sólido o granular, parte de la radiación se refleja desde la superficie de la muestra. Este reflejo espejo se llama reflejo especular y da poca información útil sobre la muestra. La mayor parte de la radiación reflejada especularmente es dirigida de nuevo hacia la fuente de energía. Otra parte de la radiación penetrará a través de la superficie de la muestra y es reflejada en varias partículas antes de que salga la muestra. Esto se conoce como reflexión difusa, y esta radiación difusamente reflejada emerge de la superficie en ángulos aleatorios de hasta 180°. Cada vez que la radiación interactúa con una partícula de muestra, los componentes químicos en la muestra pueden absorber una parte de la radiación. Por lo tanto, la radiación difusamente reflejada contiene información sobre la composición química de la muestra, como se indica por la cantidad de energía absorbida en longitudes de onda específicas.
La cantidad de radiación que penetra y sale a la superficie de la muestra se ve afectada por el tamaño y la forma de las partículas de muestra. La compensación por este efecto puede ser logrado moliendo materiales sólidos o granulares con un molino de preparación de muestra hasta obtener partículas finas y de uniforme tamaño, o aplicando correcciones matemáticas cuando el instrumento está correctamente calibrado.
8.4.1.2 Bandas de absorción en la región IR cercano
Las bandas de absorción observadas en la región cercana al IR son principalmente armónicos y combinaciones. Por lo tanto, las absorciones tienden a ser débiles en intensidad. Sin embargo, esto es realmente una ventaja, ya que las bandas de absorción que tienen suficiente intensidad para ser observados en la región cercana al IR surgen principalmente de grupos funcionales que tienen un átomo de hidrógeno unido a un carbono, nitrógeno, u oxígeno, que son grupos comunes en los componentes principales de los alimentos, como agua, proteínas, lípidos y carbohidratos. La Tabla 8.1 enumera las bandas de absorción asociadas con una serie de importantes constituyentes en los alimentos.
Las bandas de absorción en la región cercana al IR tienden a ser amplias y con frecuencia superponerse, produciendo espectros que son bastante complejos. Sin embargo, estas bandas anchas son especialmente útiles para el análisis cuantitativo. Los espectros cercanos a IR típicos de trigo, clara de huevo seca y queso son mostrados en la Figura 8.7. Tenga en cuenta que las bandas de absorción fuertes asociadas con los grupos -OH de agua que son los características dominantes en el espectro de queso, contienen 30–40% de humedad, y todavía son prominentes incluso en las muestras de trigo y clara de huevo con menor humedad. Bandas derivadas de proteínas (2060 y 2180 nm) en la muestra de trigo están parcialmente oscurecidas por un almidón que se refleja en una banda de fuerte absorción centrada a 2100 nm. Relativamente, bandas de absorción afiladas que surgen de grupos -CH en los lípidos se pueden observar a 2310, 2350 nm y 1730 nm y son claramente observables en el espectro del queso.
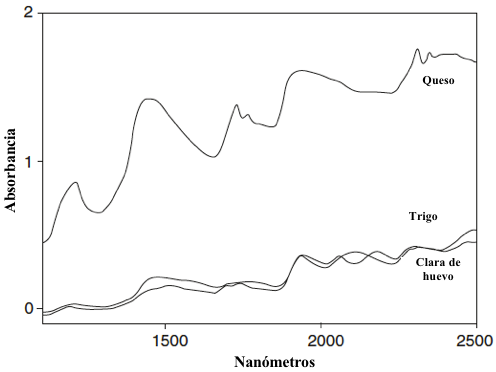
Figura 8.7 Espectro de IR cercano de queso, trigo, y huevo blanco seco ilustrado como (1/R) versus longitud de onda en nm.
8.4.2 Instrumentación
La fuente de radiación en la mayoría de los instrumentos de IR cercano es una lámpara halógena de tungsteno recubiertas por cuarzo, similar a una lámpara de proyector. Estas lámparas emiten cantidades significativas de radiación tanto en la región espectral visible como en la no visible cercanas al IR. Los detectores de semiconductores se utilizan con mayor frecuencia en instrumentos de infrarrojo cercano, con detectores de silicio utilizados en el rango de 700-1100 nm y sulfuro de plomo utilizado en la región de 1100-2500 nm. En situaciones para lo cual una respuesta rápida al cambio de intensidad de luz es necesario, como en el monitoreo en línea, indio-galio se pueden usar detectores de arseniuro (InGaAs). Muchos de los detectores InGaAs están limitados a una longitud de onda máxima de 1700 nm, aunque, detectores comerciales InGaAs con un rango extendido a longitudes de onda más largas ahora están disponibles La mayoría de los instrumentos comerciales de IR cercano usan monocromadores, en lugar de interferómetros, aunque algunos instrumentos comerciales ahora utilizan la tecnología FT. Los instrumentos basados ??en monocromadores pueden ser del tipo de escaneo, en el que una rejilla se usa para dispersar la radiación por longitud de onda, y la rejilla se gira para incidir en una sola longitud de onda (o más apropiadamente, una banda estrecha de longitudes de onda) en una muestra en cualquier momento dado. Usando este arreglo, toma varios segundos recolectar un espectro de una muestra en toda la región cercana al IR. Algunos instrumentos de escaneo rápido inciden luz sobre toda la región cercana al IR en la muestra. El reflejado de la luz transmitida luego se dirige a una rejilla fija que dispersa la luz por longitud de onda y también enfoca en un detector de matriz multicanal que mide todas las longitudes de onda a la vez. Estos instrumentos pueden obtener un espectro de una muestra en menos de 1s.

Figura 8.8 Moderno instrumento comercial de infrarrojos cercanos. (a) Thermo Scientific Antaris II. (b) Shimadzu IRTracer-100 equipado con un accesorio de esfera integradora NIR de PIKE Technologies (Fotografías cortesía de Thermo Fisher. Instrumentos científicos y científicos de Shimadzu).
Los instrumentos dedicados a aplicaciones específicas pueden usar filtros de interferencia óptica para seleccionar 6–20 discretos longitudes de onda que pueden incidir en la muestra. Los filtros se seleccionan para obtener longitudes de onda que se sabe que son absorbidas por los componentes de la muestra. El instrumento inserta filtros uno a la vez en el haz de luz para dirigir las longitudes de onda individuales de radiación sobre la muestra. Mediciones de reflexión o transmisión pueden realizarse en espectroscopía de IR cercano, dependiendo del tipo de muestra. En el modo de reflexión, usado principalmente para muestras sólidas o granulares, es deseable que se mida solo la radiación difusamente reflejada que contiene información sobre la muestra. En muchos instrumentos, esto se logra colocando el detector en un ángulo de 45° con respecto al haz IR entrante, de modo que la radiación reflejada especularmente no sea medida (Fig. 8.9a). Otros instrumentos utilizan un integrador esfera, que es una esfera metálica recubierta de oro con los detectores montados en el interior (Fig. 8.9b). Las esferas recogen la radiación difusamente reflejada que viene en varios ángulos de la muestra y la enfoca en los detectores. El componente especular se escapa de la esfera a través del mismo puerto por el cual el rayo incidente entra e incide sobre la muestra.
Las muestras a menudo se preparan empacando la comida firmemente en una celda contra una ventana de cuarzo, proporcionando una superficie lisa y uniforme desde la cual la reflexión puede ocurrir. El cuarzo no absorbe la región cercana al IR. En cada longitud de onda, la intensidad de la luz reflejada de la muestra se compara con la intensidad reflejada de una referencia que no absorbe como un material cerámico fluorocarbonado. La reflectancia (R) se calcula mediante la siguiente fórmula:
R = I /I0 (8.4)
Donde:
I = intensidad de radiación reflejada de la muestra a una longitud de onda dada
I0 = intensidad de radiación reflejada por la referencia a la misma longitud de onda
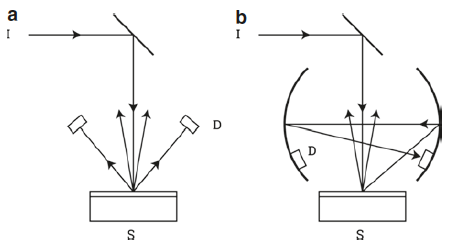
Figura 8.9 Geometrías típicas de instrumentos para medir reflectancia difusa de muestras de alimentos sólidos. La radiación del monocromador (I) es dirigida por un espejo sobre la muestra (S). Se mide la radiación difusamente reflejada directamente por detectores (D) colocados en un ángulo de 45° al rayo incidente (a) o es recogido por un esfera de integración y centrado en los detectores (b). En ambos casos, la especularidad la radiación reflejada no se mide.
Los datos de reflectancia se expresan más comúnmente como log (1/R), una expresión análoga a la absorbancia en espectroscopía de transmisión. Mediciones de reflectancia también se expresan a veces como diferencias, o derivados de los valores de reflectancia obtenidos de longitudes de onda adyacentes:
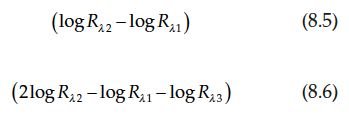
Estos valores derivados son medidas de los cambios en la pendiente del espectro, donde λ1, λ2 y λ3 son longitudes de onda adyacentes típicamente separadas por 5–20 nm, con los números más altos que representan longitudes de onda más largas.
También se pueden hacer mediciones de transmisión en la región cercana al IR, y este suele ser el método de elección para muestras líquidas. Se coloca un líquido en una cubeta de cuarzo y la absorbancia medida en las longitudes de onda de interés. Medidas de transmisión también se puede tomar de muestras sólidas, pero generalmente solo en el rango de 700–1100 nm. En esta longitud de onda las regiones de las bandas de absorción son armónicos más altos que son muy débiles, permitiendo que la radiación penetre a través de varios milímetros de una muestra sólida.
El uso de mediciones de transmisión puede minimizar el grado de preparación de la muestra necesaria. Dado que el haz de infrarrojos atraviesa toda la muestra, se reduce la necesidad de una superficie de muestra lisa y homogénea.
La energía de IR cercano puede transmitirse a través de un cable de fibra óptica a cierta distancia del monocromador o interferómetro, permitiendo la reflexión o transmisión de mediciones a realizar de forma remota desde el instrumento. Esto es muy útil para tomar medidas, en un entorno de planta de procesamiento comercial hay sondas disponibles que se pueden insertar directamente en materiales granulares a granel, o insertados en una tubería que transporta un líquido. Al igual que con el IR medio, los instrumentos de Imag8 de IR cercano son ahora disponible comercialmente. Estos instrumentos usan un detector de matriz para que una imagen digital de una muestra de alimentos se pueda obtener en varias longitudes de onda o un espectro se puede obtener de un solo píxel en una imagen digital. Esta técnica a menudo se conoce como Imag8 hiperespectrales con suficiente potencial para evaluar la heterogeneidad de las muestras o identificación de pequeñas características o contaminantes en una muestra de comida intacta.
8.4.3 Métodos cuantitativos con espectroscopía de infrarrojo
Los instrumentos infrarrojos se pueden calibrar para medir varios constituyentes en alimentos y productos agrícolas. Debido a la naturaleza superpuesta de las bandas de absorción del IR cercano, generalmente es necesario tomar medidas a dos o más longitudes de onda para cuantificar un componente alimenticio de manera confiable. Técnicas estadísticas multivariantes (quimiometría) se utilizan para relacionar datos recopilados en múltiples longitudes de onda a la concentración del componente de interés en la comida. La técnica estadística más simple utilizada es la regresión lineal múltiple (MLR), que aplica una ecuación de la siguiente forma para predecir la cantidad de un componente presente en la comida desde el espectro:
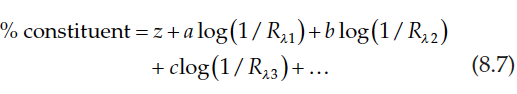
Donde cada término representa la medida espectral a una longitud de onda diferente multiplicada por un su coeficiente correspondiente. Cada coeficiente e intersección (z) se determina por análisis de regresión multivariante.
Datos de absorbancia o reflectancia derivada también se pueden usar en lugar del formato de registro (1/R). En el uso se ha encontrado que los datos de reflectancia derivada proporcionan mejores resultados en algunos casos, particularmente con muestras que pueden no tener tamaños de partícula uniformes. Otras técnicas matemáticas también están disponibles y se pueden aplicar a los datos de reflectancia para corregir los efectos del tamaño de partícula no uniforme.
Para calibrar un instrumento de infrarrojo para medición cuantitativa, se obtiene un conjunto de muestras que representan el producto a medir y contienen el componente de interés sobre el rango de interés esperado. Las muestras luego se analizan usando el método convencional de análisis (por ejemplo, para el análisis de proteínas, se usan los Métodos de Kjeldahl o Dumas y el espectro infrarrojo de cada muestra es recogido en una computadora, luego se realiza un análisis MLR para determinar las combinaciones de longitudes de onda que mejor predicen la concentración del componente de interés y los coeficientes asociados con cada longitud de onda, como se muestra en la (ecuación 8.7). En quimiometría, las técnicas como MLR, se eligen las longitudes de onda basado en la correlación estadística con el componente que se medirá. Sin embargo, los resultados siempre deben ser inspeccionados para asegurarse de que las longitudes de onda seleccionadas tienen sentido desde una perspectiva espectroscópica. Cada calibración también debe probarse utilizando un segundo conjunto de muestras, entonces, si la calibración produce resultados satisfactorios, puede usarse para análisis de rutina.
Cuando se usa MLR, a veces puede ser difícil incluir suficientes longitudes de onda para definir adecuadamente la relación entre el espectro y la composición de datos. Agregar demasiadas longitudes de onda puede "sobre ajustar" la calibración para que no se aplique bien a las muestras que no formaban parte del conjunto original. Esto puede ocurrir porque las respuestas de las longitudes de onda individuales están muy interrelacionadas. Para superar este problema y para obtener predicciones más robustas, los métodos de calibración multivariada como regresión de mínimos cuadrados parciales (PLS), y regresión de componentes principales (PCR) pueden ser usados. PLS y PCR a menudo se denominan "datos o técnicas de compresión ", ya que toman la variación espectral de todo el rango de longitudes de onda, y expresan la mayor parte de esa variación con un número menor de variables que no están correlacionadas. Estas variables luego se utilizan para desarrollar una ecuación de regresión. PLS y la PCR a menudo proporcionan mejores resultados en comparación con MLR porque pueden usar información de todo el espectro con menos riesgo de "sobre ajustar" los resultados. Por esta razón, estas dos técnicas son ahora los métodos más ampliamente utilizados para calibrar IR medio y casi todos los Instrumentos IR para análisis cuantitativos.
8.4.4 Análisis cualitativo por espectroscopía de infrarrojo
La espectroscopía de infrarrojo puede utilizarse para clasificar una muestra en uno de dos o más grupos, en lugar de proporcionar mediciones cuantitativas. Hay técnicas de clasificación, tales como análisis de componentes principales (PCA), modelado independiente suave de analogía de clase (SIMCA), o análisis discriminante, se pueden utilizar para comparar el espectro infrarrojo de una muestra desconocida con los espectros de muestras de diferentes grupos. La muestra desconocida se clasifica en el grupo al que el espectro es más similar. Si bien, esta técnica históricamente ha sido utilizada en la industria química e industrias farmacéuticas para la identificación de materias primas, es cada vez más utilizado para aplicaciones alimentarias, incluyendo la clasificación del trigo como primavera roja dura o invierno rojo duro, la identificación de jugo de naranja en muestras de diferentes fuentes, autenticación de la fuente de aceites de oliva, y discriminación de carne de res.
8.4.5 Aplicaciones de la espectroscopía de infrarrojo cercano al análisis de alimentos
Teoría y aplicaciones de la espectroscopía de IR cercano. El análisis de alimentos ha sido discutido en varias publicaciones. La técnica es ampliamente utilizada en todo el procesamiento de granos, productos de cereales e industrias de semillas oleaginosas. Técnicas de IR cercano que emplean mediciones de muestras molidas o integrales han sido adoptadas como métodos de análisis aprobados por AACC Internacional para medir proteínas en cebada, avena, centeno, trigo y harina de trigo, así como las propiedades de humedad, proteína y aceite en soja. Los métodos describen los instrumentos disponibles para hacer estas mediciones, incluida una lista de fabricantes, así como las técnicas adecuadas para preparar muestras y calibrar los instrumentos. Los instrumentos IR cercano ahora son utilizados por la agencia de inspección oficial de granos en los Estados Unidos y Canadá para medir proteína, humedad y aceite en cereales y oleaginosas.
Componentes alimentarios como proteínas y fibra dietaría puede ser exitosamente determinados en alimentos basados en cereal usando espectroscopía de IR cercano. Los instrumentos modernos y las técnicas de calibración permiten el análisis de una amplia variedad de productos, como galletas, paquetes de granola listos para el desayuno, usando la misma calibración. La espectroscopía de IR cercano también se puede utilizar para otros productos básicos y componentes alimentarios. La técnica se ha utilizado con éxito para evaluar composición y calidad de carnes rojas y productos cárnicos procesados, aves de corral y pescado. La espectroscopía de IR cercano es útil también para analizar un cantidad de productos lácteos y productos para untar no lácteos, incluyendo la medición de humedad en mantequilla y margarina, humedad, grasa y proteínas en el queso y lactosa, proteínas y humedad en la leche y el suero en polvos. Las técnicas de IR cercano también han demostrado ser prometedoras para medir azúcares totales y sólidos solubles en frutas, verduras y jugos, son utilizadas comercialmente para monitorear el contenido de azúcar maíz endulzado y pueden usarse para cuantificar sacarosa y lactosa en chocolate[6].
La espectroscopía de IR cercano también muestra potencial para medir componentes químicos específicos en un alimento que afectan su calidad de uso final, para monitorear cambios que ocurren durante el procesamiento o almacenamiento, y para saber directamente las características de procesamiento de una mercancía inherentes a su composición química. Los ejemplos incluyen la determinación del contenido de amilasa en el almidón de arroz, un determinante importante de la calidad del arroz, control del valor de peróxido en aceites vegetales, control de la degradación de los aceites para freír, y prediciendo la calidad del procesamiento del maíz.
Estos son solo algunos ejemplos de aplicaciones actuales. Si una sustancia absorbe radiación en la región cercana al IR y está presente a un nivel de algunas décimas de porcentaje o mayor, tiene potencial para ser medido por esta técnica. La principal ventaja de la espectroscopía de IR cercano es que una vez que el instrumento ha sido calibrado, se pueden medir rápidamente varios componentes de una muestra (de 30s a 2 min) simultáneamente. Para medir componentes múltiples, una ecuación de calibración para cada componente se almacena en la memoria del instrumento. Las mediciones se toman en todas las longitudes de onda, es necesario para las calibraciones y posterior en cada ecuación se resuelven para predecir los componentes de interés.
No se requiere pesado de muestra y no se utilizan reactivos peligrosos o se generan residuos químicos. También es adaptable para sistemas de medición en línea. Las desventajas incluyen el alto costo inicial de instrumentación, que puede requerir una carga muestra grande para justificar su rentabilidad, y el hecho de que es posible que sea necesario desarrollar calibraciones para cada producto medido. Además, los resultados producidos por el instrumento no pueden ser mejores que los datos utilizados para calibrar lo que hace un análisis cuidadoso de la calibración especialmente en muestras de máxima importancia.
8.5 espectroscopía Raman
8.5.1 Principios
La espectroscopía Raman es una espectroscopía vibracional complementaria a las mediciones IR. En este tipo de espectroscopía se expone una muestra a un haz de luz intenso, como un láser, y el espectro de modos vibracionales activos Raman inducidos en las moléculas de la muestra se obtiene mediante el análisis de los fotones dispersos inelásticamente. Los analitos pueden ser macrocomponentes (proteínas, lípidos, carbohidratos y agua), así como componentes presentes en menor proporción como los pigmentos carotenoides o tintes sintéticos, e incluso microorganismos o materiales de envasado en contacto con alimentos. La espectroscopía Raman puede utilizarse como herramienta para el control de la calidad, para la identificación de la composición o para la detección de adulteración, así como para la investigación básica en la elucidación de cambios estructurales o conformacionales que ocurren durante el procesamiento de alimentos[7].
Cuando un fotón de luz choca con una molécula, la colisión puede provocar la dispersión del fotón. Las moléculas en la muestra pueden excitarse y alcanzar un estado de energía virtual inestable cuando interactúan con la luz, como se muestra en la figura 8.10. Sin embargo, esta transición a un estado de alta energía en la molécula es un proceso de corta duración, y la mayoría de las moléculas se relajan de retorno a su nivel de energía fundamental que resulta en un fotón disperso de igual energía que la luz incidente. Esto se llama dispersión elástica o dispersión Rayleigh. Sin embargo, unas pocas moléculas se relajan a un mayor estado vibratorio con un cambio en la vibración y energía rotacional de la molécula causando un cambio en la longitud de onda de la radiación dispersa. Esto se llama dispersión inelástica o dispersión Raman. Para que se produzca dispersión Raman, una molécula debe sufrir un cambio en polarización de la nube de electrones de la molécula, pero no necesita sufrir un cambio en el momento dipolo. Por lo tanto, Raman puede observar vibraciones simétricas. Eso no puede ser detectado por espectroscopía de IR. Raman es complementario a la espectroscopía IR, en algunas vibraciones son solo Raman activas, algunas son solo IR activo, y algunos son ambos. Durante la dispersión Raman, fotones dispersos (aproximadamente 1 de cada 107 fotones) cambiará a longitud de onda (a una frecuencia más baja), y este cambio en frecuencia se llama líneas de Stokes o turno de Stokes. Si el estado energético final es más bajo que el estado inicial disperso los fotones cambiarán a una longitud de onda más corta (mayor frecuencia), y esto se llama líneas anti-Stokes o turno anti-Stokes. Las intensidades de las líneas de Stokes son más altas que los de las líneas anti-Stokes, y por lo tanto las líneas de Stokes generalmente se miden como Espectro Raman[8].
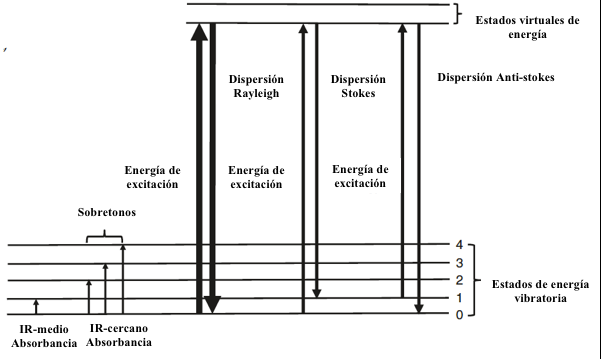
Figura 8.10 Nivel de energía diagrama de IR medio, IR cercano, Rayleigh y Dispersión Raman
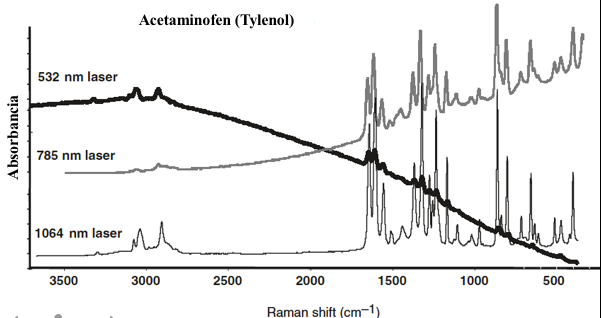
Figura 8.11 Espectro de Raman de acetaminofén (Tylenol) generado usando diferentes fuentes láser.
Un espectro típico de Raman incluye representación de la intensidad (fotones por segundo) en el eje y versus aumento de la longitud de onda (nm) o cambio de Raman (cm− 1) en el eje x. Cada banda en un espectro Raman corresponde a una vibración de un enlace químico y/o grupo funcional en la molécula como se ilustra en un espectro representativo Raman de un producto farmacéutico en Fig. 8.11. Similar a IR, la huella digital de una molécula puede ser asequible, y empleando herramientas quimiométricas se puede generar un análisis tanto cuantitativo como cualitativo, ya que la intensidad de las bandas de Raman son proporcionales a la concentración del analito[9].
La espectroscopía Raman se posiciona como una atractiva técnica, porque:
(1) Requiere poca o ninguna preparación de muestra.
(2) El agua y alcoholes son débiles dispersores Raman, que permiten la medición de muestras de agua sin ningún accesorio especial o preparación de muestra.
(3) Permite hacer mediciones a través de contenedores transparentes comunes como vidrio, cuarzo, y plástico, eliminando la necesidad de abrir contenedores para analizar los contenidos.
Para aplicaciones alimentarias de espectroscopía de Raman, el desafío de la fluorescencia de la muestra puede ser un factor limitante[10]. En general, la intensidad de la dispersión Raman es proporcional a 1/λ4, por lo que son más cortas las longitudes de onda de excitación que entregan una señal mucho más fuerte en Raman. La advertencia es que cuando se usan longitudes de onda de excitación cortas, es más probable que la fluorescencia ocurra bajo estas condiciones.
8.5.2 Instrumentación
Los espectrómetros Raman se basan en dispersivos y tecnologías de transformación de Fourier (Fig. 8.12). Cada técnica tiene sus ventajas únicas, y cada una es adecuada para tipos específicos de análisis.
Un sistema dispersivo Raman está compuesto por un láser, fuente, muestra, elemento dispersante (rejilla de difracción), detector y una computadora. Durante un típico proceso Raman de recolección de espectro, una fuente láser da un haz coherente de luz monocromática enfocada en la muestra, la luz dispersada pasa a través de un filtro de muestra que rechaza la luz dispersa de Rayleigh, el resultando en una ganancia importante en sensibilidad Raman, los fotones dispersos ingresan al monocromador, donde son separados por longitud de onda y luego recogidos por un detector que registra la intensidad de la señal Raman para cada longitud de onda. Los lásers se usan típicamente como la fuente de radiación, como la fuerza de la señal Raman es proporcional a la intensidad de la luz incidente. El uso de lásers como fuente de radiación para generar la dispersión Raman ha sido de crucial desarrollo en instrumentación Raman. Las longitudes de onda típicas son 785, 633, 532 y 473 nm. Los detectores Raman son frecuentemente matrices de fotodiodos (PDA) o cámaras con dispositivo de carga acoplada (CCD). Detectores CCD son extremadamente sensibles a la luz y contienen miles de elementos de imagen (píxeles) que adquieren el conjunto espectro a la vez en menos de un segundo. Detectores CCD permitir el uso de una potencia láser muy baja para evitar la destrucción fotoquímica de la muestra.
Los espectrómetros FT-Raman comúnmente usan un láser IR, generalmente a 1030 nm o 1064 nm. Usando láser con longitudes de onda de excitación en la región cercana al IR elimina casi por completo la fluorescencia; sin embargo, la intensidad de dispersión Raman es débil. FT-Raman utiliza un IR cercano sensible de un solo elemento de detectores como InGaAs o refrigerados por nitrógeno líquido, detectores de germanio (Ge). Un interferómetro convierte la señal de Raman en un interferograma, lo que permite al detector recoger todo el espectro simultáneamente. La aplicación de la transformada de Fourier transforma un algoritmo desde el interferograma y convierte el resultado en un espectro Raman convencional. Además, elimina la interferencia de la fluorescencia en la muestra. La espectroscopía FT-Raman, proporciona una excelente exactitud del número de onda como resultado de la calibración interna del interferómetro por un láser de helio-neón incorporado.
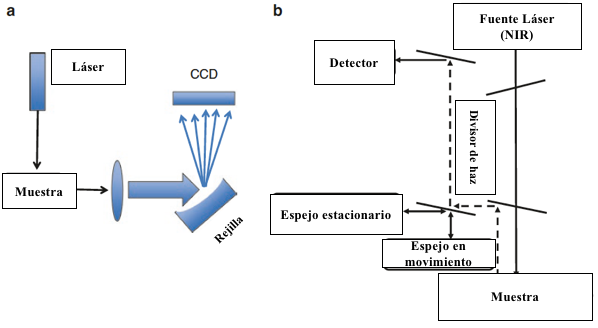
Figura 8.12 Ilustración básica de la (a) instrumentación Raman dispersiva y (b) FT-Raman.
La espectroscopía FT-Raman por ejemplo se ha explorado como un método de detección rápido para evaluar la presencia de lactosa e identificar muestras de leche en polvo adulteradas con maltodextrina (2,5-50% p/p). Las mediciones Raman pueden diferenciar fácilmente las muestras de leche en polvo, sin necesidad de prepararlas[11]. Otro ejemplo del uso de la espectroscopía FT-Raman puede utilizarse como un método de detección rápido y confiable para la evaluación de la calidad de la leche en polvo y la identificación de muestras adulteradas con suero. Las mediciones Raman pueden diferenciar fácilmente las leches en polvo sin necesidad de preparación de muestras, mientras que los métodos tradicionales de control de calidad, incluida la cromatografía líquida de alto rendimiento, son laboriosos y lentos. Se obtienen los espectros FT-Raman de muestras de leche en polvo entera, baja en grasa y desnatada y se distinguen de las muestras comerciales de leche en polvo por ejemplo. Además, el análisis exploratorio de datos de espectroscopía Raman y análisis de componentes principales (PCA) permite la separación de muestras de leche en polvo según el tipo, identificando diferencias entre muestras del mismo grupo. También se pueden clasificar las muestras de leche en polvo adulterada utilizando PCA y análisis discriminatorio de mínimos cuadrados parciales (PLS-DA[12]). Asimismo, el uso de la espectroscopía FT-Raman permite evaluar si un queso es adulterado con almidón[13].
8.5.3 Dispersión Raman mejorada mediante superficies (SERS)
Como se mencionó anteriormente, uno de los inconvenientes de la espectroscopía tradicional de Raman es el nivel muy bajo de señal Raman. Una de las técnicas más populares utilizadas para superar este problema es una superficie mejorada Dispersión Raman (SERS). Nano estructuras sobre una superficie de metal (típicamente oro o plata) mejoran la señal Raman de las moléculas de la muestra en el orden de 104-1011, lo que permite la detección en ppb o nivel de molécula única. Mecanismos simples de Raman tradicional y SERS se comparan en la Figura 8.13. Variaciones en la magnitud de la señal mejoran dependiendo de la morfología de la partícula (en las superficies rugosas se pueden proporcionar mucho más mejoras en comparación con superficies metálicas planas (lisas).
El fenómeno SERS es el resultado de una mejora de campo electromagnético producido en la superficie de metal y una mejora química debido a una carga–transferencia de interacción entre el metal y las moléculas adsorbidas. Cuando la longitud de onda de la luz incidente está cerca de una resonancia superficial excitable (colectiva excitación de electrones conductores en pequeñas estructuras de metal), moléculas adsorbidas o muy próximas a la superficie, experimentan un campo electromagnético excepcionalmente grande. Además, las transiciones electrónicas de muchos complejos de transferencia de carga entre la superficie metálica y la molécula resultan en resonancia[14].
La enorme mejora de señal lograda por SERS lo ha posicionado como un método analítico muy prometedor para el bioquímico, biomédico y farmacéutico. Las solicitudes de alimentos se han dirigido a inocuidad alimentaria para la detección de patógenos transmitidos por alimentos como alternativa al diagnóstico actual de microorganismos, brindando la posibilidad de desarrollar sensores portátiles de patógenos para la inspección de alimentos en el sitio. Otras aplicaciones de SERS incluyen la detección de contaminantes de alimentos (pesticidas y residuos de antibióticos) y adulteración (melanina, colorantes alimentarios ilegales y mico-toxinas). También or ejemplo esta herramienta permite hacer una medición rápida y confiable de los factores cualitativos del tomate y sus productos. La comparación de los espectros SERS con los espectros Raman normales ha demostrado que SERS tiene un privilegio en la medición de carbohidratos y proteínas como una técnica eficaz, rápida y precisa[15]. Además se ha propuesto esta herramienta como un método rápido y preciso para detectar patógenos como Alternaria alternata en productos alimentarios como en jugo de pera[16]. También en la detección de contaminantes alimentarios la SERS se ha considerado una herramienta importante, debido a su alta sensibilidad rapidez y capacidades de interpretación de huellas dactilares que explican su competencia para detectar una molécula hasta un solo nivel. Por lo que se propone para la detección directa e indirecta de contaminantes químicos y microbianos únicos y múltiples en alimentos, productos alimenticios y agua. Por ejemplo la presencia de antibióticos, pesticidas, adulterantes alimentarios, toxinas, bacterias y virus[17].
8.6 Tecnología portátil y de mano
Las técnicas de espectroscopía vibratoria son ideales para ser utilizadas como instrumentos portátiles o de mano. Su simplicidad, velocidad, selectividad y habilidad para operar sin una previa preparación de muestra los hace ideales para ser utilizado fuera del laboratorio para el proceso de monitoreo en entornos desafiantes. Un solo espectrómetro se puede usar para verificar la identidad de materiales a granel, control de contaminación, procesos de control, y conforme las especificaciones finales del producto. Los instrumentos de campo tienen que tolerar condiciones duras, mantener la confiabilidad y precisión, ser fáciles de operar, de alimentación por batería, ligero con un diseño ergonómico, diseño e interfaz de usuario intuitiva, los accesorios deben ser robustos, con limitada o nula preparación de la muestra requerida y capaz de desarrollar análisis oportunamente (Fig. 8.14).
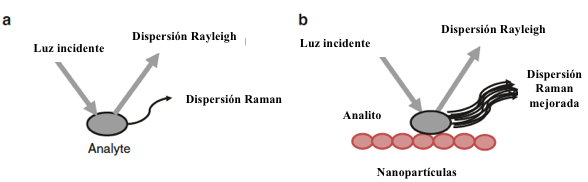
Figura 8.13 Comparación de (a) mecanismo tradicional Raman y (b) SERS.

Figura 8.14 Espectrómetros vibracionales portátiles/de mano disponibles comercialmente. (a) Agilent 4300 handheld FTIR, (b) FTIR portátil Agilent 4500, (c) computadora de mano Thermo microPhazir IR cercano, (d) computadora de mano Progeny ™ 1064 nm Analizador Raman de Rigaku Analytical Devices, y (e) espectrómetro Raman portátil DeltaNu ReporteR.
La ventaja de los espectrómetros portátiles de infrarrojos medios (en comparación con IR cercano) es la señal fundamental más alta, permitiendo la detección de bajos niveles del analito y su capacidad para conferir huellas digitales a determinados componentes. Sin embargo, si una muestra contiene agua, su fuerte absorción a IR medio puede plantearnos información inválida. IR cercano permite el análisis sin ninguna preparación de la muestra. El más usado en el muestreo para sólidos es la reflectancia difusa, mientras que transflectancia (transmisión combinada y reflectancia) y la transmisión son configuraciones adecuadas para análisis de líquidos. Aunque la señal de IR cercano es de 10 a 1000 veces más baja que las bandas de IR medio, las absorciones más bajas permiten que el haz de IR cercano penetre más profundamente en la muestra, resultando en un análisis más representativo. Las ventajas de los instrumentos portátiles Raman para campo es que su implementación incluye poca o ninguna preparación de muestra, permite obtener resultados sin contacto y no destructivos de la muestra, mientras la respuesta Raman es relativamente débil en el agua para permitir la medición de soluciones acuosas. Análisis de IR cercano y Raman permiten mediciones a través de películas de vidrio y plástico. Espectrómetros vibratorios portátiles y de mano, son técnicas atractivas de huellas digitales de componentes para varias aplicaciones que incluyen alimentos, productos farmacéuticos, petroquímicos, y aplicación de la ley.
8.7 Resumen
La espectroscopía IR mide la absorción de radiación en el IR cercano (λ = 0.8–2.5 μm) o en el IR medio (λ = 2.5–15 μm), regiones aplicables a moléculas en alimentos u otras sustancias. En IR la radiación se absorbe a medida que las moléculas cambian de vibración sus niveles de energía. Un resumen de lo más importante. Se presentan las características de las técnicas de espectroscopía. En la Tabla 8.2. La espectroscopía de IR medio es especialmente útil para el análisis cualitativo, como la identificación específica de grupos funcionales presentes en una sustancia. Los grupos funcionales absorben diferentes frecuencias de radiación, permitiendo que los grupos sean identificados desde un espectro de una muestra. El análisis cuantitativo también se puede lograr mediante espectroscopía de IR medio, con el análisis de leche siendo una aplicación importante La espectroscopía de infrarrojo cercano es utilizado más ampliamente para aplicaciones cuantitativas, utilizando medidas de transmisión o reflexión difusa que pueden tomarse directamente de alimentos sólidos.
Mediante el uso de técnicas estadísticas multivariadas, los instrumentos de infrarrojo pueden calibrarse para medir las cantidades de varios componentes en una muestra de alimentos basado en la cantidad de radiación IR absorbida a longitudes de onda específicas. La espectroscopía de IR medio, IR cercano y Raman requieren mucho menos tiempo para realizar análisis cuantitativos que muchas técnicas químicas convencionales o cromatográficas.
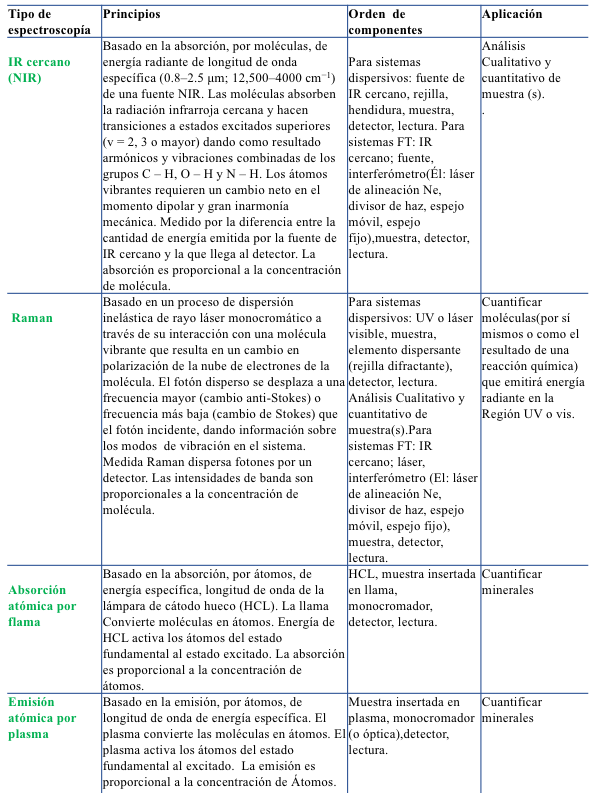
Tabla 8.2 Comparación de los métodos de espectroscopía comunes en el análisis de alimentos.
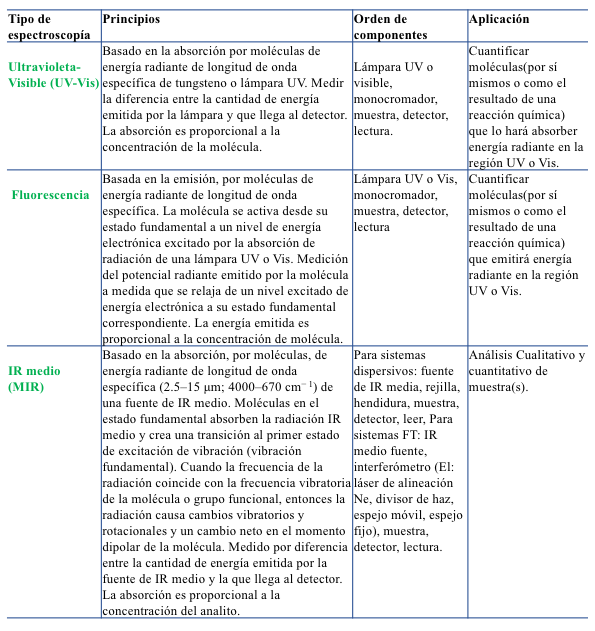
Continuación de la tabla…
8.8 Preguntas de estudio
1. Describa los factores que afectan la frecuencia de vibración de un grupo funcional molecular, y las frecuencias de radiación que absorbe. Además, explique cómo la absorción fundamental y las absorciones de armónicos de una molécula están relacionados.
2. Describa los componentes esenciales de un espectrómetro FT-IR medio y su función, y compare el funcionamiento del instrumento FT con un instrumento dispersivo ¿Qué ventajas tiene FT? ¿Los instrumentos tienen espectrofotómetros IR dispersivo?.
3. Describa las similitudes y diferencias entre espectroscopía IR medio y espectroscopía Raman.
4. De los tres antioxidantes, hidroxitolueno butilado (BHT), hidroxianisol butilado (BHA), y galato de propilo, ¿de cuál se espera tener una fuerte banda de absorción IR en la región espectral de 1700–1750 cm− 1? Buscar estos compuestos en un libro de referencia si usted desconoce su estructura química.
5. Describa las dos formas en que la radiación es reflejada de un material sólido o granular. ¿Qué tipo de radiación reflejada es útil para hacer mediciones cuantitativas en sólidos por espectroscopía de infrarrojo cercano? Como son los Instrumentos de reflectancia de IR cercano diseñados para seleccionar el componente deseado de radiación reflejada?.
6. Describa los pasos involucrados en la calibración de un Instrumento de reflectancia de infrarrojo cercano para medir contenido proteico de la harina de trigo. ¿Por qué suele ser necesario para realizar mediciones a más de una longitud de onda?.
Referencias
[1] Lu, X., and Rasco, B. A. (2012). Determination of Antioxidant Content and Antioxidant Activity in Foods using Infrared Spectroscopy and Chemometrics: A Review. Critical Reviews in Food Science and Nutrition, 52(10), 853–875. https://doi.org/10.1080/10408398.2010.511322
[2] Dufour, Éric. (2011). Recent Advances in the Analysis of Dairy Product Quality Using Methods Based on the Interactions of Light with Matter. International Journal of Dairy Technology. 64. 153 - 165. 10.1111/j.1471-0307.2010.00665.x.
Mcgoverin, Cushla & Ruangratanakorn, Jittima & Downey, Gerard & Manley, Marena. (2010). Review: The application of near infrared spectroscopy to the measurement of bioactive compounds in food commodities. Journal of Near Infrared Spectroscopy. 18. 87-111. 10.1255/jnirs.874.
[3] Karoui, Romdhane & Downey, Gerard & Blecker, Christophe. (2010). Mid-Infrared Spectroscopy Coupled with Chemometrics: A Tool for the Analysis of Intact Food Systems and the Exploration of Their Molecular Structure−Quality Relationships − A Review. Chemical reviews. 110. 6144-68. 10.1021/cr100090k.
[4] Hollas J.M. Modern Spectroscopy. Ed 4. John Wiley and Son,Ltd. 2004. ISBN 0470844159
[5] Yadav L.D.S. Organic Spectroscopy.Norwell,MA,USA:Kluwer Academic Publisher;2005.
[6] Jimare Benito, Maria & Bosch-Ojeda, Catalina & Rojas, F.. (2008). Process Analytical Chemistry: Applications of Near Infrared Spectrometry in Environmental and Food Analysis: An Overview. Applied Spectroscopy Reviews. 43. 452-484. 10.1080/05704920802031382.
[7] Li-Chan, Eunice. (1996). The Application of Raman Spectroscopy in Food Science. Trends in Food Science & Technology - TRENDS FOOD SCI TECHNOL. 7. 361-370. 10.1016/S0924-2244(96)10037-6.
Qin, Jianwei & Chao, Kuanglin & Kim, moon seok & Cheng, Yu-Che. (2013). Authentication of Milk Powder using Raman Scattering Spectroscopy and Imaging. American Society of Agricultural and Biological Engineers Annual International Meeting 2013, ASABE 2013. 1. 10.13031/aim.20131591839.
[8] Application of Raman spectroscopy technique to agricultural products quality and safety determination. 35. 2567-2572. 10.3964/j.issn.1000-0593(2015)09-2567-06.
[9] Liu, Yan-de & Liu, Tao & Sun, Xudong & Ouyang, Ai-guo & Hao, Yong. (2010). Application of Raman Spectroscopy Technique to Food Quality and Safety Determination. Guang pu xue yu guang pu fen xi = Guang pu. 30. 3007-12. 10.3964/j.issn.1000-0593(2010)11-3007-06.
[10] Yang, Danting & Ying, Yibin. (2011). Applications of Raman Spectroscopy in Agricultural Products and Food Analysis: A Review. Applied Spectroscopy Reviews. 46. 539-560. 10.1080/05704928.2011.593216.
Liu, Y.-D & Jin, T.-T. (2015).
[11] Rodrigues Júnior, Paulo & Oliveira, Kamila & Almeida, Carlos & De Oliveira, Luiz Fernando & Stephani, Rodrigo & Pinto, Sandra & Carvalho, Antonio & Perrone, Ítalo. (2016). FT-Raman and Chemometric Tools for Rapid Determination of Quality Parameters in Milk Powder: Classification of Samples for the Presence of Lactose and Fraud Detection by Addition of Maltodextrin. Food Chemistry. 196. 584-588. 10.1016/j.foodchem.2015.09.055.
[12] Almeida, Mariana & Oliveira, Kamila & Stephani, Rodrigo & De Oliveira, Luiz Fernando. (2011). Fourier-transform Raman analysis of milk powder: A potential method for rapid quality screening. Journal of Raman Spectroscopy. 42. 1548 - 1552. 10.1002/jrs.2893.
[13] Oliveira, Kamila & Callegaro, Layce & Stephani, Rodrigo & Almeida, Mariana & De Oliveira, Luiz Fernando. (2016). Analysis of Spreadable Cheese by Raman Spectroscopy and Chemometric Tools. Food Chemistry. 194. 441-446. 10.1016/j.foodchem.2015.08.039.
[14] Almeida, Mariana & Oliveira, Kamila & Stephani, Rodrigo & De Oliveira, Luiz Fernando. (2011). Fourier-transform Raman analysis of milk powder: A potential method for rapid quality screening. Journal of Raman Spectroscopy. 42. 1548 - 1552. 10.1002/jrs.2893.
[15] Oliveira, Kamila & Callegaro, Layce & Stephani, Rodrigo & Almeida, Mariana & De Oliveira, Luiz Fernando. (2016). Analysis of Spreadable Cheese by Raman Spectroscopy and Chemometric Tools. Food Chemistry. 194. 441-446. 10.1016/j.foodchem.2015.08.039.
[16] Pan, Ting-tiao & Sun, Da-Wen & Pu, Hongbin & Wei, Qing-Yi & Xiao, Wang. (2017). Detection of A. alternata from pear juice using surface-enhanced Raman spectroscopy based silver nanodots array. Journal of Food Engineering. 215. 10.1016/j.jfoodeng.2017.07.019.
[17] Guo, Yahui & Girmatsion, Mogos & Li, Hung-Wing & Xie, Yunfei & Yao, Weirong & Qian, He & Abraha, Bereket & Mahmud, Abdu. (2020). Rapid and ultrasensitive detection of food contaminants using surface-enhanced Raman spectroscopy-based methods. Critical Reviews in Food Science and Nutrition. 1-14. 10.1080/10408398.2020.1803197.
Autores:
Eduardo Ochoa Hernández
Nicolás Zamudio Hernández
Lizbeth Guadalupe Villalon Magallan
Mónica Rico Reyes
Pedro Gallegos Facio
Gerardo Sánchez Fernández
Rogelio Ochoa Barragán